
����Ŀ��Na2O2����ǿ�����ԣ���������Ư��֯����Ʒ����ˡ���ά�ȡ�
��1������ͼ��ʾʵ�飬��Ӧ�Ļ�ѧ����ʽΪ_______________��ʵ����������Թ�������Һ�еμӷ�̪��Һ��������___________________________��
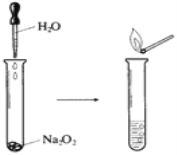
��2��������ͨ��������������Na2O2��ĩ������������ȼ�ա�ԭ����Na2O2��H2O��CO2��Ӧ��������CO2��Ӧ�Ļ�ѧ����ʽΪ______________________������״���·�Ӧ������5.6LO2����ת�Ƶ��ӵ����ʵ���Ϊ______mol��
�������ƣ�CaO2����һ�ְ�ɫ������������ˮ�Ĺ��壬��ɱ���������㷺���ڹ��߱��ʡ�������������ˮ�����ȷ��档��ҵ�����������£�
����NH4Cl��Һ�м���Ca��OH��2��
���ڵڢٲ������ɵIJ����м���30%H2O2����Ӧ����CaO28H2O������
�۾����»������ˣ�ˮϴ�õ�CaO28H2O������ˮ����õ�CaO2��
���������գ�
��3���ڢٲ���Ӧ�Ļ�ѧ����ʽΪ_____________________��
��4�������п�ѭ��ʹ�õ�������_____________________��
��5������CaO28H2O�Ƿ�ϴ���ķ�����___________��
��6����֪CaO2��350��Ѹ�ٷֽ�����CaO��O2����ͼ��ʵ���Ҳⶨ��Ʒ��CaO2������װ�ã��г�װ��ʡ�ԣ���

����ȡ��Ʒ������m g������������ΪV mL�����������Ʒ��CaO2����������Ϊ________������ĸ��ʾ�����������Ƶĺ���Ҳ�����������ⶨ����Ҫ�ⶨ����������______________________��
���𰸡� 2Na2O2+2H2O=4NaOH+O2�� �ȱ�����ɫ 2Na2O2+2CO2=2Na2CO3+O2 0.5 2NH4Cl+Ca��OH��2=2NH3H2O+CaCl2 NH4Cl ȡ�������һ��ϴ��Һ���Թ��У��μ����������ữ����������Һ���۲��Ƿ������ɫ���������������ɫ������֤��û��ϴ�Ӹɾ�������ϴ�Ӹɾ� ![]() ��9V/1400m ��Ʒ�����ͷ�Ӧ������������������ɣ�
��9V/1400m ��Ʒ�����ͷ�Ӧ������������������ɣ�
����������1���������ƺ�ˮ��Ӧ�����������ƺ����������ݻ�ѧ��Ӧ�IJ�����ȷ���������������м��ԣ���ʹ��̪��ʾ��ɫ���Ҳ�����������ɫ��ȥ��
��2���������ƺ�ˮ�Լ�������̼��Ӧ������������������ÿ����1mol������ת��2mol���Ӽ���������5.6LO2��ת�Ƶ��ӵ����ʵ�����
��3���ڢٲ����Ȼ�狀��������Ʒ������ֽⷴӦ����һˮ�ϰ����Ȼ��ƣ�
��4���ڢٲ����Ȼ�鱗μӷ�Ӧ���ڢڲ��������Ȼ�泥�
��5��ʵ�����������ữ����������Һ���������ӣ�
��6�����ݹ������ƺ�����֮��Ĺ�ϵʽ���㣻�������Ƶĺ���Ҳ�����������ⶨ����Ҫ�ⶨ������������Ʒ�����ͷ�Ӧ�����������
��1���������ƺ�ˮ��Ӧ�����������ƺ���������2Na2O2+2H2O=4NaOH+O2�������Թ�������Һ�еμӷ�̪��Һ����ϵ�ʼ��ԣ���Һ��죬�������������������ԣ��ʽ���ҺƯ�ף������������ȱ�����ɫ��
��2����Ϊ�������ƺ�ˮ�Լ�������̼��Ӧ������������������������ȼ�ԣ����й������ƺͶ�����̼��Ӧ����̼���ƺ���������2Na2O2+2CO2=2Na2CO3+O2��ÿ����1mol������ת��2mol���ӣ��������������ʵ�����5.6L��22.4L/mol=0.25mol�����ת��0.5mol���ӣ�
��3���ڢٲ����Ȼ�狀��������Ʒ������ֽⷴӦ����һˮ�ϰ����Ȼ��ƣ���Ӧ����ʽΪ2NH4Cl+Ca��OH��2=2NH3H2O+CaCl2��
��4���ڢڲ���Ӧ�У��Ȼ��ơ�˫��ˮ��һˮ�ϰ���ˮ��Ӧ����CaO28H2O���Ȼ�泥���Ӧ����ʽΪCaCl2+H2O2+2NH3H2O+6H2O=CaO28H2O��+2NH4Cl���ڢٲ����Ȼ�鱗μӷ�Ӧ���ڢڲ��������Ȼ�泥����Կ���ѭ��ʹ�õ�������NH4Cl��
��5��ʵ�����������ữ����������Һ���������ӣ��������û��ϴ�Ӹɾ�����ϴ��Һ�м��������ữ����������ҺӦ���а�ɫ����������鷽���ǣ�ȡ�������һ��ϴ��Һ���Թ��У��μ����������ữ����������Һ���۲��Ƿ������ɫ���������������ɫ������֤��û��ϴ�Ӹɾ�������ϴ�Ӹɾ���
��6���賬����������Ϊxg������ݷ���ʽ��֪
2CaO2![]() 2CaO+O2��
2CaO+O2��
144g 22.4L
xg 0.001L
144g��22.4L=xg��0.001L
���x=9V/1400
����������=9V/1400m��100%=9V/14m%��
����������Ƶĺ���Ҳ�����������ⶨ������Ҫ�ⶨ������������Ʒ�����ͷ�Ӧ�����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ�ϵ�ؿ���ʹ���ں���ɻ��ϣ��䷴Ӧԭ��ʾ��ͼ����ͼ�������й�����ȼ�ϵ�ص�˵������ȷ����

A. ��װ�ý���ѧ��ת��Ϊ����
B. Ϊ�����ӵ������ȣ����Խ��缫̼����ôֲڶ��
C. ����Ǩ�Ʒ��缫a���������缫b���������Һ���缫a
D. �õ�ص��ܷ�Ӧ��2H2+O2=2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У����������������ʵ���
A.��ȫȼ�ղ���ֻ�ж�����̼��ˮB.����������ˮ
C.�����Ƿǵ����D.���ӵ�ͨʽΪCnH2n+2������������ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������[KAl(SO4)2��12H2O] ���������������й㷺��;������ˮ�ľ�������ֽ��ҵ����ʩ������ʳƷ��ҵ�ķ��ͼ��ȡ������������ķ��ϡ�������(��Al�� Al2O3������SiO2��FeO ��xFe2O3)���Ʊ������������������£��ش��������⣺
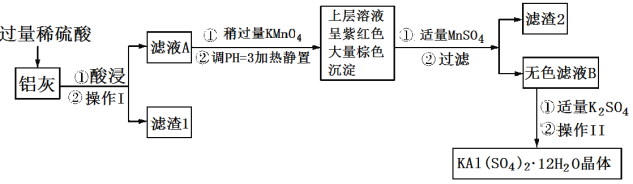
(1)������ˮ��ԭ����______________________________(�����ӷ���ʽ��ʾ)��
(2)��������________��������������Ũ����__________�����ˡ�__________�����
(3)������ҺA���Ƿ����Fe2�����Լ���________________(ֻ��һ���Լ�)��
(4)������Ͷ������������Һ����������Ļ�ѧ����ʽ��_______________________������ҺA�м��������ط�����Ӧ�����ӷ���ʽΪ(��������MnO4��ת��ΪMn2��)��________________��
(5)��֪����pH��3�����������£�MnO![]() ����Mn2����Ӧ����MnO2������MnSO4������Ӧ�����ӷ���ʽΪ��________������2���е�������_______________��
����Mn2����Ӧ����MnO2������MnSO4������Ӧ�����ӷ���ʽΪ��________������2���е�������_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ���ҵ�Թ��ú���ᷢչ������Ҫ���塣�����ܱ������еķ�Ӧ��N2(g)��3H2(g)![]() 2NH3(g)����673 K��30 MPa�£�n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ��ͼ��ʾ������������ȷ����
2NH3(g)����673 K��30 MPa�£�n(NH3)��n(H2)��ʱ��仯�Ĺ�ϵ��ͼ��ʾ������������ȷ����

A. ��a������Ӧ���ʱȵ�b��С
B. ��c����Ӧ�ﵽƽ��
C. ��d(t1ʱ��)�͵�e(t2ʱ��)��n(N2)��һ��
D. ��e����Ӧ�ﵽƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[��ѧ����ѡ��5���л���ѧ����]��Ȳ���ڴ��������¿ɷ���ż����Ӧ����ΪGlaser��Ӧ��
2R��C��C��H![]() R��C��C��C��C��R+H2
R��C��C��C��C��R+H2
�÷�Ӧ���о����ͷ�����ϡ������ӻ�ѧ�ȷ��������Ҫ��ֵ������������Glaser��Ӧ�Ʊ�������E��һ�ֺϳ�·�ߣ�

�ش��������⣺
��1��B�Ľṹ��ʽΪ______��D �Ļ�ѧ����Ϊ______��
��2���������ķ�Ӧ���ͷֱ�Ϊ______��______��
��3��E�Ľṹ��ʽΪ______����1 mol E�ϳ�1,4���������飬��������Ҫ��������_______mol��
��4�������![]() ��Ҳ�ɷ���Glaserż����Ӧ���ɾۺ���þۺϷ�Ӧ�Ļ�ѧ����ʽΪ_____________________________________��
��Ҳ�ɷ���Glaserż����Ӧ���ɾۺ���þۺϷ�Ӧ�Ļ�ѧ����ʽΪ_____________________________________��
��5�����㻯����F��C��ͬ���칹�壬�������ֻ�����ֲ�ͬ��ѧ�������⣬��Ŀ��Ϊ3:1��д������3�ֵĽṹ��ʽ_______________________________��
��6��д����2�����Ҵ�Ϊԭ�ϣ��������Լ���ѡ���Ʊ�������D�ĺϳ�·��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������ʢٵ�ˮ ���廯����Һ �������Ƶ���ˮ ���Ȼ�þ��Һ����ʹʪ��ĵ��۵⻯����ֽ�����������( )
A.�٢�B.�ڢ�C.�ڢ�D.�٢ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2C2O4Ϊ��Ԫ���ᡣ20��ʱ������һ��c(H2C2O4)+ c(HC2O4�C)+ c(C2O42�C)=0.100 mol��L�C1��H2C2O4��NaOH�����Һ����Һ�в����������ʵ���Ũ����pH�ı仯������ͼ��ʾ������ָ����Һ���������ʵ���Ũ�ȹ�ϵһ����ȷ����

A. pH=2.5����Һ�У�c(H2C2O4)+c(C2O42�C)��c(HC2O4�C)
B. c(Na+)=0.100 mol��L�C1����Һ�У�c(H+)+c(H2C2O4)=c(OH�C)+c(C2O42�C)
C. c(HC2O4�C)=c(C2O42�C)����Һ�У�c(Na+)��0.100 mol��L�C1+c(HC2O4�C)
D. pH=7����Һ�У�c(Na+)<2c(C2O42�C)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com