
| A. | ②⑥⑧ | B. | ①②⑥ | C. | ③⑦⑧ | D. | ①⑤⑨ |
分析 ①NaAlO2水溶液中,除了NaAlO2本身,水也含氧原子;
②过氧化钠和水的反应中,氧元素的价态由-1价变为0价;
③NO2和N2O4之间存在转化,方程式2NO2?N2O4;
④92235U+01n$\stackrel{裂变}{→}$3890Sr+54136U+1001n净产生的中子为10-1=9个;
⑤1个氧气分子得到4个电子生成氢氧根离子;
⑥根据n=cV计算出硝酸的物质的量,然后利用N原子守恒计算溶液中N原子数目;
⑦氯气与水的反应为可逆反应;
⑧12g石墨和C60的混合物中含有12gC原子,根据n=$\frac{m}{M}$计算出C的物质的量,然后计算出含有质子总数;
⑨胶体微粒是氢氧化铁的集合体.
解答 解:①NaAlO2水溶液中,除了NaAlO2本身,水也含氧原子,故溶液中含有的氧原子的个数大于2NA个,故①错误;
②过氧化钠和水的反应中,氧元素的价态由-1价变为0价,故当生成0.1mol氧气时,转移0.2NA个电子,故②正确;
③NO和O2反应方程式为2NO+O2=2NO2,根据方程式知,2molNO与1molO2恰好完全反应生成2molNO2,但NO2和N2O4之间存在转化,方程式2NO2?N2O4,所以产物分子数小于2NA,故③错误;
④92235U+01n$\stackrel{裂变}{→}$3890Sr+54136U+1001n净产生的中子为10-1=9个,则235g核素92235U发生裂变反应净产生的中子(01n)数为9NA,故④错误;
⑤氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为4NA,故⑤错误;
⑥1L 0.5mol/L稀硝酸中含有硝酸的物质的量为:0.5mol/L×1L=0.5mol,含有0.5molN原子;当生成标况下2.24LNO(0.1mol)时,根据N原子守恒可知溶液中的氮原子数的物质的量为:0.5mol-0.1mol=0.4mol,含有N原子数为0.4NA个,故⑥正确;
⑦氯气与水的反应为可逆反应,不能进行彻底,故转移的电子数小于NA个,故⑦错误;
⑧12g石墨和C60的混合物中含有12gC,含碳C原子的物质的量为:$\frac{12g}{12g/mol}$=1mol,1molC原子中含有6mol质子,含有的质子总数一定为6NA,故⑧正确;
⑨胶体微粒是氢氧化铁的集合体,将100mL0.1mol•L-1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒小于0.01NA,故⑨错误;
故选A.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系,试题有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉和淀粉酶混合后微热 | |
| B. | 用蘸有质量分数为75%的酒精棉花球擦皮肤 | |
| C. | 用紫外线光灯照射病房 | |
| D. | 用福尔马林浸动物标本 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
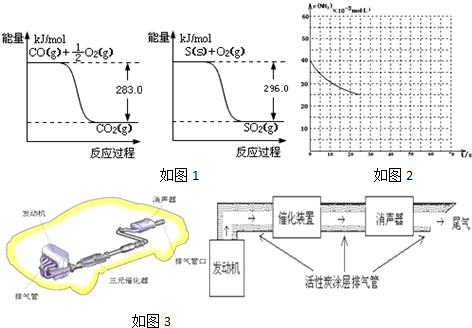
| A. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(2Q1-2Q2+Q3) kJ•mol-1 | |
| B. | S(s)+2CO(g)═SO2(g)+2C(s)△H=(Q1-Q3) kJ•mol-1 | |
| C. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(Q1-2Q2+Q3) kJ•mol-1 | |
| D. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(2Q1-Q2+2Q3) kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CuO)(mol) | 0.080 | 0.060 | 0.040 | 0.020 | 0.020 | 0.020 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、K+、OH-、NO3-、CO32-、SO42-.为了进一步确认,对该溶液进行实验检测:
某100mL溶液中含有的部分离子浓度大小如图所示,该溶液可能还含有Fe3+、Ba2+、K+、OH-、NO3-、CO32-、SO42-.为了进一步确认,对该溶液进行实验检测:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com