
【题目】某溶液可能含有Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-中的几种,为确定其成分,完成了如下实验(已知:3NO3-+8Al+5OH-+2H2O ![]() 3NH3↑+ 8AlO2- )
3NH3↑+ 8AlO2- )
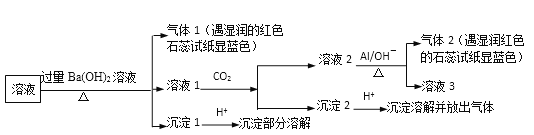
根据实验现象,所得结论错误的是
A.沉淀1加酸部分溶解,则含Mg2+和SO42-B.可能含Na+、Cl-
C.沉淀2加酸溶解,则含Al3+D.气体1遇水显碱性,则含NH4+
【答案】C
【解析】
试样溶液中加入过量Ba(OH)2并加热,生成的气体1能使湿润的红色石蕊试纸变蓝色,说明气体1是NH3,则试样中含有NH4+;
向滤液中通入CO2,得到溶液2、沉淀2,溶液2中加入Al,生成气体2,该气体能使湿润红色石蕊试纸变蓝色,说明含有气体2是NH3,根据已知条件知,溶液2中含有NO3-,根据元素守恒知,原溶液中含有NO3-;
滤液1中通入CO2,得到沉淀2,向沉淀2中加入酸,沉淀溶解并放出气体,说明沉淀2是碳酸钡等难溶性碳酸盐;
沉淀1加入酸后,沉淀部分溶解,硫酸钡不溶于酸,说明原来溶液中含有SO42-,能和过量Ba(OH)2反应生成能溶于酸的沉淀,根据离子知,该沉淀为Mg(OH)2,所以溶液中含有Mg2+,结合题给选项分析解答。
根据上述分析可知,
A. 沉淀1加酸部分溶解,试样中肯定存在Mg2+和SO42-,A项正确;
B. 依据分析,不能确定溶液中是否存在Na+、Cl-,B项正确;
C. 通过以上分析知,试样中不能确定是否含有Al3+,C项错误;
D. 遇水显碱性的气体为氨气,则推知溶液中含NH4+,D项正确;
答案选C。


科目:高中化学 来源: 题型:
【题目】在100 ℃、常压下,将乙醇变为蒸气,然后与乙烯以任意比例混合,混合气体的体积为V L。使该混合气体完全燃烧,需消耗相同条件下的氧气的体积是
A. 2V L B. 2.5V L C. 3V L D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象或事实可用同一原理解释的是
A.新制的氨水、氯水放置时间较久而变质
B.![]() 能使溴水和品红溶液褪色
能使溴水和品红溶液褪色
C.![]() 和
和![]() 溶液使酸性高锰酸钾溶液的紫色褪去
溶液使酸性高锰酸钾溶液的紫色褪去
D.浓硫酸和浓盐酸长期暴露在空气中浓度降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.用序号按要求回答下列问题:
(1)下列各种物质:①H2O②NH3③KOH④Na2O2⑤MgCl2⑥Ne,不存在化学键的是________;只存在离子键的是________;含有非极性键的离子化合物的是________。
(2)下列变化过程:①碘的升华②NaCl固体溶于水③O2溶于水④HCl气体溶于水⑤烧碱熔化⑥氯化铵受热分解,化学键没有被破坏的是________;仅破坏离子键的是________;仅破坏共价键的是________,既破坏离子键,又破坏共价键的是________。
(3)Na2O2的电子式为________________________,用电子式表示H2O的形成过程:________________________________________________。
Ⅱ.有A、B、C、D、E五种微粒。已知:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后,其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。请回答:
(1)写出这五种微粒的符号:
A______,B______,C______,D______,E______。
(2)B微粒的结构示意图为____________,C微粒的结构示意图为____________。
(3)A的单质与EB溶液反应的离子方程式为______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.物质的类别和核心元素的化合价是研究物质性质的两个基本视角。请根据下图所示,回答下列问题:

(1)X的化学式为____________。
(2)W的浓溶液与铜单质在加热条件下可以发生化学反应,反应的化学方程式为______________________。
(3)已知SO3是一种酸性氧化物,则SO3与NaOH溶液反应的离子方程式为__________________________________。
(4)欲制备Na2S2O3(硫代硫酸钠),从氧化还原反应角度分析,合理的是_______(填序号)。
A.Na2S+S B.Na2SO3+S C.Na2SO3+Na2SO4 D.SO2+Na2SO4
(5)将X与Y混合,可生成淡黄色固体,该反应的氧化产物与还原产物的质量之比为_____。
Ⅱ.如图所示:图中每一方格表示有关的一种反应物或生成物,其中A、C为无色气体,请填写下列空白:
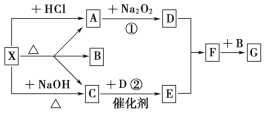
(1)物质X可以是_____________,C是______,F是_______。
(2)反应①的化学方程式是________________________________________。反应②的化学方程式是___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中第VIIA族元素的单质及其化合物的用途广泛。完成下列填空:
(1)与氯元素同族的短周期元素的原子核外有_________种不同能量的电子,写出其最外层电子的轨道表示式____________________________。
(2)不能作为溴、碘元素非金属性(原子得电子能力)递变规律的判断依据是______(填序号)。
a.IBr中溴为-1价 b.HBr、HI的酸性
c.HBr、HI的热稳定性 d.Br2、I2的熔点
(3)已知:AlF3的熔点为1040℃,AlCl3在178℃升华。从物质结构的角度解释两者熔点相差较大的原因:_____________________________________
(4)HClO有很好的杀菌消毒效果。为增强氯水的杀菌能力,可以用饱和氯水与小苏打反应来达到目的,试用平衡移动原理解释其原因:__________________________________
(5)卤素单质及其化合物在许多性质上都存在递变规律,请从物质结构角度说明下列递变规律的原因。
①熔点按F2、Cl2、Br2、I2的顺序依次升高,原因是__________________________。
②还原性按Cl-、Br-、I-的顺序依次增大,原因是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 原子核外电子排布式为1s2的原子与核外电子排布式为1s22s2的原子化学性质相似
B. Fe3+的最外层电子排布式为3s23p63d5
C. 基态铜原子的最外层的电子排布图: ![]()
D. 基态碳原子的最外层电子排布图:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃的分子球棍模型,据此回答下列问题:
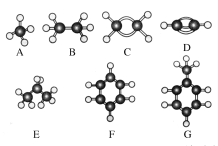
(1)常温下含碳量最高的气态烃是________(填对应字母);
(2)能够发生加成反应的烃有________(填数字)种;
(3)一卤代物种类最多的是________(填对应字母);
(4)写出实验室制取D的化学方程式________________________________;
(5)写出F发生溴代反应的化学方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是苯和溴的取代反应的实验装置图,其中A为具有支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量的铁屑粉。填写下列空白:

(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中发生反应的化学方程式(有机物写结构简式)______________;
(2)试管C中苯的作用是______________。反应开始后,观察D和E两支试管,看到的现象分别是______________,_____________;
(3)反应2 min~3 min后,在B中的氢氧化钠溶液里可观察到的现象是____________;
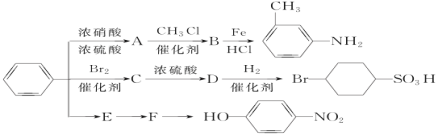
(4)苯是一种重要的化工原料,以下是用苯作为原料制备某些化合物的转化关系图:
已知:a.RNO2 ![]() RNH2
RNH2
b.苯环上原有的取代基对新导入的取代基进入苯环的位置有显著影响。
c.![]()
①A转化为B的化学方程式是____________________;
②在“苯![]() E
E![]() F
F![]()
![]() ”的反应中所选试剂a是__________,b是___________,c是__________。
”的反应中所选试剂a是__________,b是___________,c是__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com