
| A. | 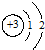 | B. | 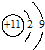 | C. | 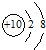 | D. | 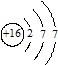 |
分析 在原子结构示意图中,质子数即核电荷数等于核外电子数,核电荷数为118则核外也应有118个电子;核外电子在分层排布时,应遵循各电子层最多容纳电子数2n2,n为电子层数,且次外层电子数不超过18个,最外层不超多8个,以此解答该题.
解答 解:A.先排内层,再排外层,K层应为2个电子,故A错误;
B.最外层不能超过8个,应为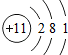 ,故B错误;
,故B错误;
C.符合排布规则,故C正确;
D.先排内层,再排外层,应为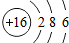 ,故D错误.
,故D错误.
故选C.
点评 本题考查基态原子的电子排布的判断,是基础性试题的考查,侧重对学生基础知识的巩固和训练,该题的关键是明确各电子层最多容纳电子数2n2,n为电子层数,且次外层电子数不超过18个,最外层不超多8个,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 丙烷分子的球棍模型图: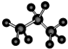 | B. | TNT的分子式:C7H5N3O6 | ||
| C. | 乙烯分子的比例模型: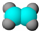 | D. | 苯乙醛的结构简式: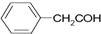 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | I2+SO2+2H2O═H2SO4+2HI | B. | 2FeCl2+Cl2═2FeCl3 | ||
| C. | 2FeCl3+2HI═2FeCl2+2HCl+I2 | D. | FeCl2+I2═FeI2+Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
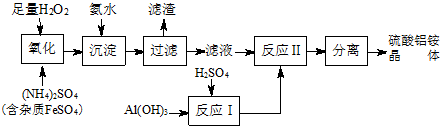
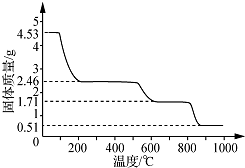
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
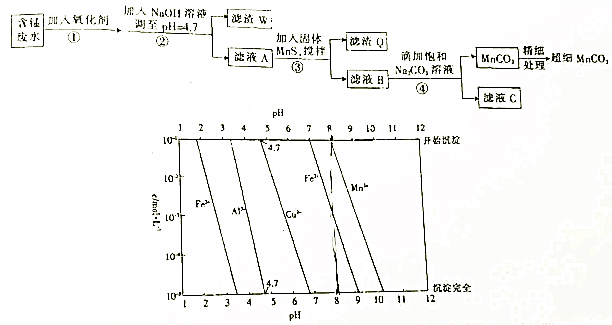
查看答案和解析>>
科目:高中化学 来源:2017届山西省高三上期中化学试卷(解析版) 题型:选择题
在1L含0.2molKOH、0.1molNaAlO2和0.1 mol Ba(NO3) 2 的混合溶液中,逐滴加入浓度为0.1 mol/L 的H 2 SO 4 溶液,下列图像中能表示反应产生的沉淀的物质的量和所加入硫酸溶液的体积关系是(已知AlO2-和Ba2+可以大量共存)

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com