
����Ŀ������г���A��R����Ԫ�������ڱ���λ�ã�
���� | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | E | R | F | |||||
3 | A | C | D | H | I | G | ||
4 | B |
��1��д��R���ʷ��ӵĵ���ʽ ��
��2��A��C��D����Ԫ�ص��������Ӧ��ˮ�����м�����ǿ�������ѧʽ����
��3��A��B��C����Ԫ�ص������Ӱ����Ӱ뾶�ɴ�С��˳������Ϊ �� ����Ԫ�ص����ӷ��ű�ʾ����
��4��д��A�ĵ�����ˮ��Ӧ�����ӷ���ʽ ��
��5��XԪ����A��R����Ԫ���е�һ�֣�X��ԭ�Ӻ�����14�����ӣ�2.7gX��������ȼ��ʱ����������2.4g��X�������������������������Һ��Ӧ��Ҳ�������ᷴӦ��X��Ԫ�ط����� �� ��λ��Ԫ�����ڱ���λ����
���𰸡�
��1��![]()
��2��NaOH
��3��K+��Na+��Mg2+
��4��2Na+2H2O=2Na++OH��+H2��
��5��Al����3���ڵڢ�A��
���������⣺����Ԫ�������ڱ��е�λ��֪����A��R�ֱ���Na��K��Mg��Al��C��O��Cl��Si��S��NԪ�أ���1��R�����ǵ��������������е�ԭ��֮�乲��3�Ե��ӣ���ÿ��Nԭ�ӻ���1���µ��Ӷԣ��������ӵ���ʽΪ ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ����2��Ԫ�صĽ�����Խǿ��������������ˮ�������Խǿ��������Na��Mg��Al�����������ֽ���Ԫ������������ˮ���������ǿ����NaOH�����Դ��ǣ�NaOH����3�����Ӳ���Խ�����Ӱ뾶Խ���Ӳ�ṹ��ͬ�����ӣ����Ӱ뾶����ԭ�������������С��������Ԫ�ؼ����ӵ��Ӳ�����ࡢ�����Ӻ�þ���ӵ��Ӳ�ṹ��ͬ����Naԭ������С��Mg������������Ԫ�����Ӱ뾶��С˳����K+��Na+��Mg2+ �� ���Դ��ǣ�K+��Na+��Mg2+����4��A������Na��Na��ˮ��Ӧ����NaOH�����������ӷ���ʽΪ2Na+2H2O=2Na++OH��+H2�������Դ��ǣ�2Na+2H2O=2Na++OH��+H2������5��X��ԭ�Ӻ�����14�����ӣ�X�������������������������Һ��Ӧ��Ҳ�������ᷴӦ����������������ǿ�ᡢǿ����Һ����X��AlԪ�أ�Alλ�ڵ������ڵ�IIIA�壬���Դ��ǣ�Al���������ڵ�IIIA�壮
����2��Ԫ�صĽ�����Խǿ��������������ˮ�������Խǿ��������Na��Mg��Al�����������ֽ���Ԫ������������ˮ���������ǿ����NaOH�����Դ��ǣ�NaOH����3�����Ӳ���Խ�����Ӱ뾶Խ���Ӳ�ṹ��ͬ�����ӣ����Ӱ뾶����ԭ�������������С��������Ԫ�ؼ����ӵ��Ӳ�����ࡢ�����Ӻ�þ���ӵ��Ӳ�ṹ��ͬ����Naԭ������С��Mg������������Ԫ�����Ӱ뾶��С˳����K+��Na+��Mg2+ �� ���Դ��ǣ�K+��Na+��Mg2+����4��A������Na��Na��ˮ��Ӧ����NaOH�����������ӷ���ʽΪ2Na+2H2O=2Na++OH��+H2�������Դ��ǣ�2Na+2H2O=2Na++OH��+H2������5��X��ԭ�Ӻ�����14�����ӣ�X�������������������������Һ��Ӧ��Ҳ�������ᷴӦ����������������ǿ�ᡢǿ����Һ����X��AlԪ�أ�Alλ�ڵ������ڵ�IIIA�壬���Դ��ǣ�Al���������ڵ�IIIA�壮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���淴ӦCO + H2O(g) ![]() CO2 + H2���ﵽƽ��ʱ��K =
CO2 + H2���ﵽƽ��ʱ��K =![]() ��K�dz�����ֻ���¶��йأ���Ũ���ء�
��K�dz�����ֻ���¶��йأ���Ũ���ء�
��1��830Kʱ������ʼʱ��c (CO) = 2 mol/L��c (H2O) = 3 mol/L��ƽ��ʱCO��ת����Ϊ60%��ˮ������ת����Ϊ______________��KֵΪ______________��
��2��830K����ֻ����ʼʱc (H2O)��Ϊ6 mol/L����ˮ������ת����Ϊ____________��
��3����830Kʱ����ʼŨ��c (CO) = a mol/L��c (H2O) = b mol/L��H2��ƽ��Ũ��c (H2) = c mol/L��
��a��b��c֮��Ĺ�ϵʽ��____________________________________��
�ڵ�a = bʱ��a = __________c��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и����л����У�һ������ͬϵ����ǣ� ��
A.C2H4��C2H2B.C2H2��C6H6
C.C3H8��C5H12D.C2H4��C4H8
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ᴿ��ʵ���У����в�����ȷ����( )
A. ����ʱ�ò���������©���ڵ�Һ�壬�Լ��ٹ���
B. ��������������ʱ����Ҫ�ò���������
C. ���������г��ֽ϶�������ʱ��Ӧֹͣ����
D. ����Һ���ɺ�ֹͣ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4NH3(g)+ 5O2(g)![]() 4NO(g)+ 6H2O(g) ��1L���ܱ������н��У�30s��ˮ���������ʵ���������0.45 mol����˷�Ӧ��ƽ������v��X������Ӧ����������ʻ������������ʣ��ɱ�ʾΪ�� ��
4NO(g)+ 6H2O(g) ��1L���ܱ������н��У�30s��ˮ���������ʵ���������0.45 mol����˷�Ӧ��ƽ������v��X������Ӧ����������ʻ������������ʣ��ɱ�ʾΪ�� ��
A. v��NH3��= 0.1 mol��L1��s-1 B. v��O2��= 0.01 mol��L1��s-1
C. v��NO��= 0.01 mol��L1��s-1 D. v��H2O��= 0.045 mol��L1��s-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ж�����Ԫ��A��B��C��D��E��
��֪���ٳ����£�AԪ�صĵ����ڿ�����Ũ�����У����涼���������ܵ�����Ĥ��
��BԪ�ص�ԭ��������AԪ�ش���ԭ�ӵĴ����ĵ�������������������2����
��E��Aͬ���ڣ�C��D��E����Ԫ���γɵĵ��ʻ���ɷ�����ͼ��ʾ�ķ�Ӧ��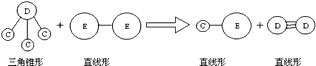
��ش��������⣺
��1��д��AԪ�������������NaOH��Һ��Ӧ�����ӷ���ʽ����
��2��DԪ�ص�ԭ�ӽṹʾ��ͼ�ǣ���
��3��BԪ����EԪ�ص�����������ˮ���������ǿ�����û�ѧʽ��ʾ��������
��4�����û�ѧ����ʽ��ʾEԪ�صĵ����ڹ�ҵ�ϵ�һ����Ҫ��;�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ��Һ���ܴ����������������
A. Mg2+��NH4+��C1-��OH- B. Na+��AlO2-��CO32-��OH-
C. Ca2+��Fe2+��H+��NO3- D. Fe3+��K+��SCN-��SO42-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�����������ʵ������ȡ�������ǣ� ��
A.�����Ȼ�狀���ʯ�ҹ���
B.����Ũ��ˮ
C.Ũ��ˮ�μӵ���ʯ����
D.���ȹ����Ȼ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com