

| 物质 | Na | S | Al2O3 |
| 熔点/℃ | 97.8 | 115 | 2050 |
| 沸点/℃ | 892 | 444.6 | 2980 |
| mg |
| 102g/mol |
| m |
| 102 |
| m |
| 51 |
| ||
| v×10-3L |
| 1000m |
| 51v |
| 1000m |
| 51v |


科目:高中化学 来源: 题型:
| A、Na+、Mg2+、SO42- |
| B、K+、H+、CO32- |
| C、Fe3+、SO42-、NO3- |
| D、Ba2+、Al3+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、SiO32-、NO3- |
| B、NH4+、Al3+、SO42- |
| C、Na+、OH-、SO42- |
| D、Na+、CH3COO-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、废旧电池可埋入土壤,作为肥料 |
| B、电池工作时电子从正极沿导线流向负极 |
| C、电池工作时一定没有氧化还原反应发生 |
| D、氢氧燃料电池,通H2的电极为电池的负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(NH3) |
| n(CO2) |
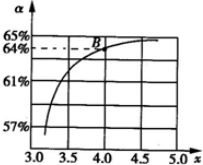

查看答案和解析>>
科目:高中化学 来源: 题型:
时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | 1.00 | 1.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |

查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用溴的四氯化碳溶液除去甲烷中混有的少量乙烯气体 |
| B、向淀粉溶液中加入稀硫酸,加热几分钟,冷却后再加入少量新制Cu(OH)2浊液,加热,没有红色沉淀生成,说明淀粉还没有发生水解 |
| C、用硝酸酸化的AgNO3溶液检验CCl4中是否含有氯元素 |
| D、红热的铜丝可以和乙醇发生置换反应产生氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com