
| A. | 通过蒸馏,分离苯和硝基苯的混合物 | |
| B. | 电解AlCl3,可得金属铝 | |
| C. | 将MgCl2溶液蒸干,可得无水MgCl2 | |
| D. | 用过滤的方法,从碘水中提取碘 |
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案科目:高中化学 来源: 题型:选择题
| A. | 氯水的颜色呈浅黄绿色,是因为氯水中含有Cl2 | |
| B. | 新制氯水能使红色布条褪色,说明氯水中含HClO | |
| C. | 向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+ | |
| D. | 活性炭和氯水都具有漂白作用,且漂白的化学原理相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向(NH4)2Fe(SO4)2溶液中加入过量氢氧化钠:NH4++Fe2++30H-=NH3•H2O+Fe(OH)2↓ | |
| B. | 向明矾溶液中滴加Ba(0H)2溶液至SO42- 恰好完全沉淀:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ | |
| C. | 向澄清石灰水中加入过量碳酸氢钠溶液:Ca2++2OH-+2HCO3-=CaCO3↓+2H2O+CO32- | |
| D. | 向酸性FeC12溶液中加入H2O2:2Fe2++2H2O2=2Fe3++O2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝不易发生化学反应 | |
| B. | 铝的氧化物易发生还原反应 | |
| C. | 铝不易被氧化 | |
| D. | 铝易被氧化为氧化铝,氧化铝膜具有保护内部铝的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知:下表为25℃时某些弱酸的电离平衡常数.
已知:下表为25℃时某些弱酸的电离平衡常数.| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7Ka2=4.7×10-11 |
| A. | 25℃时,相同浓度的NaHCO3溶液的碱性大于NaClO溶液 | |
| B. | 图象中a点的导电能力小于c点 | |
| C. | 图象 I代表CH3COOH溶液的稀释 | |
| D. | 图象中a点酸的总浓度大于b点酸的总浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
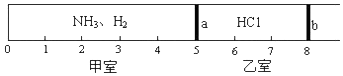
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ①③ | C. | ①②③⑤ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
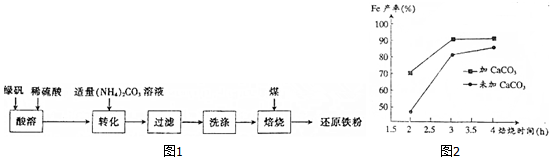
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com