
在5L的密闭容器中充入2mol A气体和1mol B气体,在一定条件下发生反应:2A(g)+B(g)⇌2C(g),达到平衡时,在相同温度下测得容器内混合气体的压强是反应前的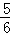 ,试求:
,试求:
(1)平衡时A的浓度
(2)A的转化率.
考点:
化学平衡的计算.
专题:
化学平衡专题.
分析:
依据化学平衡三段式列式计算,设A转物质的量x,
2A(g)+B(g)⇌2C(g)
初始物质的量 2 mol 1 mol 0
转化物质的量 x 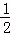 x x
x x
平衡物质的量 2 mol﹣x 1 mol﹣ x x
x x
依据气体压强之比等于气体物质的量之比计算分析.
解答:
解:恒温恒容时,混合气体的压强是反应前的 ,说明混合气体的物质的量也是反应前的
,说明混合气体的物质的量也是反应前的 .设A转化了物质的量x
.设A转化了物质的量x
2A(g)+B(g)⇌2C(g)
初始物质的量 2 mol 1 mol 0
转化物质的量 x  x x
x x
平衡物质的量 2 mol﹣x 1 mol﹣ x x
x x
则(2 mol﹣x)+(1mol﹣ x)+x
x)+x
= ×(2 mol+1 mol)
×(2 mol+1 mol)
x=1 mol
(1)A的浓度为c(A)=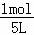 =0.2mol•L﹣1;
=0.2mol•L﹣1;
答:平衡时A的浓度为0.2mol•L﹣1;
(2)A的转化率α(A)=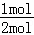 ×100%=50%,答:A的转化率为50%.
×100%=50%,答:A的转化率为50%.
点评:
本题考查了化学平衡计算方法的分析应用,主要考查浓度、转化率的计算分析,注意气体压强之比等于气体 物质的量之比,题目较简单.


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案科目:高中化学 来源: 题型:
两只串联的电解池,左池放CuSO4溶液,右池放一定量的某硝酸盐稀溶液,电解时,当左池析出1.6g铜时,右池析出0.45g固体,则右池中的溶质为()
A. AgNO3 B. NaNO3 C. Mg(NO3)2 D. Al(NO3)3
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下硝酸铵受热分解的未配平化学方程式为NH4NO3——HNO3+N2+H2O,在反应中被氧化与被还原的氮原子数之比为( )
A.5∶3 B.5∶4
C.1∶1 D.3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
在2NO2⇌N2O4的可逆反应中,下列状态属于平衡状态的是( )
|
| A. | υ正=υ逆≠0时的状态 | B. | NO2全部转变成N2O4的状态 |
|
| C. | c(NO2)=c(N2O4)的状态 | D. | N2O4不再分解的状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
高温下,某反应达平衡,平衡常数K=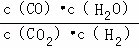 .恒容时,温度升高,H2浓度减小.下列说法正确的是( )
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
|
| A. | 该反应的焓变为正值 |
|
| B. | 恒温恒容下,增大压强,H2浓度一定减小 |
|
| C. | 升高温度,逆反应速率减小,平衡常数K增大 |
|
| D. | 该反应化学方程式为CO+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学在实验室里过滤一种浑浊溶液,发现滤出的液体仍浑浊,他检查实验装置发现漏斗外壁没有水,滤纸也未出现破损或小漏洞,则造成实验失败的原因可能是下列操作中的( )
|
| A. | 滤纸高出漏斗边缘的部分未剪掉 |
|
| B. | 滤纸与漏斗之间有气泡未被排掉 |
|
| C. | 倾倒液体时液面高于滤纸边缘 |
|
| D. | 过滤时玻璃棒靠在一层滤纸一边 |
查看答案和解析>>
科目:高中化学 来源: 题型:
食盐中含有一定量的镁、铁等杂质,加碘盐中碘的损失主要是由于杂质、水分、空气中的氧气以及光照、受热而引起的。已知:氧化性:
 >Fe3+>I2;还原性:
>Fe3+>I2;还原性: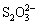 >I-;
>I-;
3I2+6OH-
 +5I-+3H2O;
+5I-+3H2O;
KI+I2 KI3
KI3
(1)某学习小组对加碘盐进行如下实验:取一定量某加碘盐(可能含有KIO3、KI、Mg2+、Fe3+),用适量蒸馏水溶解,并加稀盐酸酸化,将所得溶液分为3份。第一份试液中滴加KSCN溶液后显红色;第二份试液中加足量KI固体,溶液显淡黄色,用CCl4萃取,下层溶液显紫红色;第三份试液中加入适量KIO3固体后,滴加淀粉试剂,溶液不变色。
①加KSCN溶液显红色,该红色物质是_________(用化学式表示);CCl4中显紫红色的物质是___________________(用电子式表示)。
②第二份试液中加入足量KI固体后,反应的离子方程式为___________________________、______________________________________。
(2)KI作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。
写出潮湿环境下KI与氧气反应的化学方程式:_____________________________。
将I2溶于KI溶液,在低温条件下,可制得KI3·H2O。该物质作为食盐加碘剂是否合适?______(填“是”或“否”),并说明理由________________________________________。
(3)为了提高加碘盐(添加KI)的稳定性,可加稳定剂减少碘的损失。下列物质中有可能作为稳定剂的是___________________。
A.Na2S2O3 B.AlCl3 C.Na2CO3 D.NaNO2
(4)对含Fe2+较多的食盐(假设不含Fe3+),可选用KI作为加碘剂。请设计实验方案,检验该加碘盐中的Fe2+:__________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com