
| A. | ①和② | B. | ②和③ | C. | ③和④ | D. | ②③⑥ |
分析 ①化合物是不同元素组成的纯净物,液氨是氨气属于化合物、液氯是单质;
②依据混合物是不同物质组成的分析;
③电解质是水溶液中或熔融状态下导电的化合物;
④胶体的本质特征是分散质微粒直径在1nm-100nm间;
⑤钠盐应电离出钠离子与酸根离子;
⑥酸跟碱完全中和生成的盐属于正盐,不含有酸中的氢离子,也不含有碱中的氢氧根离子.
解答 解:①液态氨气属于纯净的化合物、液氯是单质,干冰、碘化银均为化合物,故①错误;
②氢氟酸是HF的水溶液,盐酸是氯化氢水溶液,氨水为氨气水溶液均为混合物,纯碱为纯净物,故②错误;
③明矾、小苏打、醋酸、次氯酸,符合电解质概念,均为电解质,故③正确;
④烟、云、雾、豆浆的分散质粒子直径在1nm~100nm间,属于胶体,故④正确;
⑤Na2CO3、NaHCO3、Na2SiO3均为钠盐,Na2O2没有酸根所以不是盐,是氧化物,故⑤错误;
⑥NaCl、Na2CO3、NaF均为正盐,NaHSO4含有酸中的氢离子属于酸式盐,故⑥错误;
故选C.
点评 本题考查了化学基本概念的理解和应用,熟悉混合物、化合物、单质、胶体、电解质、盐等概念的分析即可判断,掌握物质的组成是解题关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①④⑤ | D. | ①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 的沸点比
的沸点比 高,原因
高,原因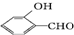 形成分子内氢键,而
形成分子内氢键,而 形成分子间氢键,分子间氢键使分子间作用力增大.
形成分子间氢键,分子间氢键使分子间作用力增大.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤⑧ | B. | ①③④⑤⑧ | C. | ①③④⑧ | D. | 以上均不对 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件,该小组同学为探究中毒原因进行了如下实验:
实验小组同学看到一则报道:某造纸厂误将槽车中漂白液(NaCl和NaClO的混合液)倒入盛放饱和KAl(SO4)2溶液的池中,造成中毒事件,该小组同学为探究中毒原因进行了如下实验:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积一定相等 | B. | 分子数一定相等 | ||
| C. | 质量一定相等 | D. | 物质的量一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10mL | B. | 20mL | C. | 40mL | D. | 60mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com