
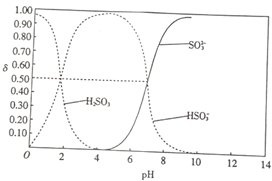
 25℃时,向100mL 1mol•L-1H2SO3溶液中逐渐滴入1mol•L-1的NaOH溶液,含硫物质的分布分数δ(平衡时某物质的浓度与各物质浓度之和的比)与pH的关系如图所示(已知:pKs=-lgK,25℃时,H2SO3的pKa1=1.85,pKa2=7.19).下列说法不正确的是( )
25℃时,向100mL 1mol•L-1H2SO3溶液中逐渐滴入1mol•L-1的NaOH溶液,含硫物质的分布分数δ(平衡时某物质的浓度与各物质浓度之和的比)与pH的关系如图所示(已知:pKs=-lgK,25℃时,H2SO3的pKa1=1.85,pKa2=7.19).下列说法不正确的是( )| A. | pH=1.85时,c(H2SO3)=c(HSO3-) | |
| B. | pH=6时,c(Na+)>c(HSO3-)>c(SO32-) | |
| C. | pH=7.19时,c(Na+)+c(H+)=c(HSO3-)+2c(SO3-)+c(OH-) | |
| D. | 加入150mLNaOH溶液时,3c(Na+)=2c(H2SO3)+2c(HSO3-)+2c(SO32-) |
分析 25℃时,向100mL 1mol•L-1H2SO3溶液中逐渐滴入1mol•L-1的NaOH溶液,发生的反应为:H2SO3+NaOH=NaHSO3,NaHSO3+NaOH=Na2SO3+H2O
A.含硫酸物质的分布分数δ为0.50时c(H2SO3)=c(HSO3-);
B.PH=6时溶液中主要的离子是HSO3-和SO32-,溶液显酸性;
C.pH=7.19时溶液中为Na2SO3和HNaHSO3的混合溶液,溶液中存在电荷守恒;
D.加入150mLNaOH溶液时溶液中为Na2SO3和NaOH的混合溶液,溶液中存在物料守恒分析判断;
解答 解:A.含硫酸物质的分布分数δ为0.50时c(H2SO3)=c(HSO3-),pH=1.85,故A正确;
B.PH=6时溶液中主要的离子是HSO3-和少量SO32-,溶液显酸性,c(Na+)>c(HSO3-)>c(SO32-),故B正确;
C.pH=7.19时溶液中为Na2SO3和HNaHSO3的混合溶液,溶液中存在电荷守恒c(Na+)+c(H+)=c(HSO3-)+2c(SO32-)+c(OH-),故C正确;
D.加入150mLNaOH溶液时溶液中为Na2SO3和NaOH的混合溶液,溶液中存在物料守恒分析可知3c(Na+)>2c(H2SO3)+2c(HSO3-)+2c(SO32-),故D错误;
故选D.
点评 本题考查了离子浓度大小比较,电解质溶液中电荷守恒、物料守恒的分析判断,注意曲线变化的特征和溶液成分判断,掌握基础是解题关键,题目难度较大.


 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:选择题
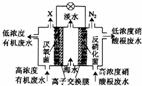 一种三室微生物燃料电池污水净化系统原理如图所示,图中废水有机物可用 C6H10O5表示.下列有关该燃料电池的说法错误的是( )
一种三室微生物燃料电池污水净化系统原理如图所示,图中废水有机物可用 C6H10O5表示.下列有关该燃料电池的说法错误的是( )| A. | 中间室中的 Cl-向左室移动 | |
| B. | 左、右两室溶液混合后所得溶液的酸性:反应前<反应后 | |
| C. | X气体为CO2 | |
| D. | 左边离子交换膜为阴离子交換膜,右边离子交换膜为阳离子交換膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
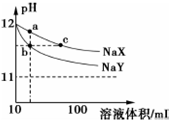 常温下,体积均为10mL、pH均为12的NaX和NaY两种钠盐溶液,分别加水稀释,pH随溶液体积的变化如图所示.下列叙述错误的是( )
常温下,体积均为10mL、pH均为12的NaX和NaY两种钠盐溶液,分别加水稀释,pH随溶液体积的变化如图所示.下列叙述错误的是( )| A. | 相同温度下,电离平衡常K(HX)<K(HY) | |
| B. | b、c两点溶液中水的电离程度相同 | |
| C. | a点溶液中:c(H+)+c(HX)=c(OH-) | |
| D. | b、c两点溶液中Na+的物质的量:nb(Na+)<nc(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M一定是第VIA族元素 | B. | M的最高价氧化物为RO2 | ||
| C. | M的气态氢化物一定能形成氢键 | D. | M的气态氢化物溶于水可能显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可燃冰是一种清洁能源 | B. | CH4•nH2O是一种离子化合物 | ||
| C. | 可燃冰在常温常压下能稳定存在 | D. | 可燃冰是天然气冷却后得到的固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
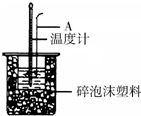 利用如图装置测定中和热的实验步骤如下:
利用如图装置测定中和热的实验步骤如下:| 温度 实验次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 25.0 | 25.2 | 28.5 | ||
| 2 | 24.9 | 25.1 | 28.3 | ||
| 3 | 25.5 | 26.5 | 31.8 | ||
| 4 | 25.6 | 25.4 | 29.0 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铍的原子失电子能力比镁弱 | |
| B. | Tl(OH)3 和Al(OH)3一样都属于两性氢氧化物 | |
| C. | 硫化氢比硒化氢稳定 | |
| D. | 锂与氧气在点燃的条件下生成氧化锂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | ||||||
| D | E | F | |||||
| C | I | G | H |
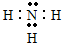
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
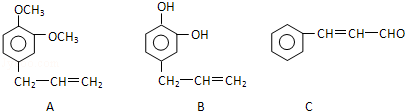
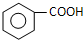 +
+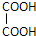 则C9H8O的结构简式为
则C9H8O的结构简式为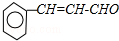 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com