
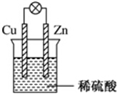
 如果烧杯中最初装入的是500mL 2mol•L-1的稀硫酸溶液,构成铜锌原电池(见图,假设产生的气体没有损失),当在标准状况下收集到11.2L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度分别为(溶液体积变化忽略不计)c(H2SO4)=1mol•L-1,c(ZnSO4)=1mol•L-1.
如果烧杯中最初装入的是500mL 2mol•L-1的稀硫酸溶液,构成铜锌原电池(见图,假设产生的气体没有损失),当在标准状况下收集到11.2L的氢气时,则此时烧杯内溶液中溶质的物质的量浓度分别为(溶液体积变化忽略不计)c(H2SO4)=1mol•L-1,c(ZnSO4)=1mol•L-1. 分析 在标准状况下收集到11.2L的氢气,即0.5mol,转移1mol电子,正极反应为2H++2e-=H2↑,负极上的电极反应式为:Zn→Zn2++2e-,结合电极方程式计算.
解答 解:根据正极反应:2H++2e-=H2↑,当在标准状况下收集到11.2L即0.5mol的氢气时,转移电子是1mol,减少的氢离子为1mol,消耗硫酸0.5mol,则剩余硫酸的物质的量为2mol/L×0.5L-0.5mol=0.5mol,所以剩余的硫酸的浓度为1mol/L,
负极上的电极反应式为:Zn→Zn2++2e-,当转移电子1mol时,生成锌离子的量为0.5mol,所以c(ZnSO4)=$\frac{0.5mol}{0.5L}$=1mol/L,
故答案为:1;1.
点评 本题考查原电池知识,为高频考点,侧重于学生的分析、计算能力的考查,注意把握电极方程式的书写,为解答该题的关键,题目难度不大.


 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| A. | 在恒温恒容下,当容器中压强不再变化时,该反应达到了化学平衡状态 | |
| B. | 已知c(CO2)•c(H2)=c(CO)•c(H2O),则温度为800℃ | |
| C. | 该反应的△H>0 | |
| D. | 在830℃时,发生上述反应,达到平衡时CO2的转化率为50% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酒精在实验台上着火,迅速用水熄灭 | |
| B. | 实验室里电线失火,首先要断开电源 | |
| C. | 浓硫酸沾到皮肤上,用大量水冲洗,再用醋酸洗 | |
| D. | 腐蚀性药品溅到眼睛里,迅速送往医院治疗 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:1 | C. | 1:1 | D. | 2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4HSO4溶液中加入少量NaOH稀溶液:NH4++OH-=NH3•H2O | |
| B. | Ca(ClO)2溶液中通入过量的二氧化硫气体:ClO-+SO2+H2O=HClO+HSO3- | |
| C. | 酸性高锰酸钾溶液中滴入少量过氧化氢:2MnO4-+7H2O2+6H+=2Mn2++6O2↑+10H2O | |
| D. | 为缓解胃酸过多,服含NaHCO3的抗酸药:HCO3-+H+=H2O+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com