
| A. | 铁是人体健康、植树生长所必须的元素之一,缺铁时可用补充FeSO4的方法补铁 | |
| B. | 在采煤作业中,把炸药和干冰放在一起,既能增强爆炸威力,又能防止火灾 | |
| C. | 氢氧燃料电池已用于航天飞机,燃料电池的能量转化率理论上可达100% | |
| D. | 聚乙烯塑料可用于制作餐具 |
分析 A.Fe为构成血红蛋白的重要元素;
B.干冰可隔绝空气,不燃烧、不支持燃烧,且爆炸时气体增多;
C.燃料电池的能量转化率较高,但不能完全转化为电能;
D.聚乙烯塑料无毒.
解答 解:A.Fe为构成血红蛋白的重要元素,则缺铁时可用补充FeSO4的方法补铁,亚铁离子易被吸收和利用,故A正确;
B.干冰可隔绝空气,不燃烧、不支持燃烧,且爆炸时气体增多,则把炸药和干冰放在一起,既能增强爆炸威力,又能防止火灾,故B正确;
C.燃料电池的能量转化率较高,但不能完全转化为电能,还转化为热能,则能量转化率不能达到100%,故C错误;
D.聚乙烯塑料无毒,则可用于制作餐具,故D正确;
故选C.
点评 本题考查物质的性质及用途,为高频考点,把握物质的性质、发生的反应、性质与用途等为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.


科目:高中化学 来源: 题型:解答题
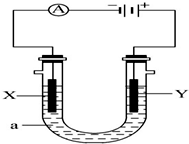 电解原理在化学工业中有广泛应用.如图表示一个电解池,X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞溶液,请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子及其离子的核外电子层数等于该元素所在的周期数 | |
| B. | 元素周期表中从IIIB族到IIB族 10个纵行的元素都是金属元素 | |
| C. | 除氦外的稀有气体原子的最外层电子数都是8 | |
| D. | 同一元素的各种同位素的物理性质、化学性质均相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
序号 | 时间/min 物质的量/mol 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| 1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 |
| 2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
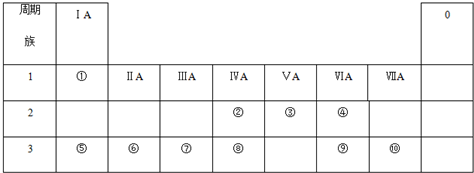
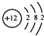
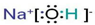
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
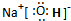 ,所含有的化学键有离子键、极性共价键;它属于离子化合物(填“离子”或“共价”).
,所含有的化学键有离子键、极性共价键;它属于离子化合物(填“离子”或“共价”).查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com