
A.次氯酸钙Ca(ClO)2是氧化剂,被还原
B.HCl是还原剂,被氧化
C.氯气是氧化产物,氯化钙是还原产物
D.氧化产物与还原产物的质量比为1∶1
 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:
试完成下列问题:
(1)上述实验中理论上最多可制得Ca(ClO)2多少克?
(2)实验中所得到的Ca(ClO)2的质量明显小于理论值,试简要分析其可能原因,并写出可能涉及的化学方程式。
查看答案和解析>>
科目:高中化学 来源:2014届山东省济宁市高二12月质量检测化学试卷(解析版) 题型:选择题
下列说法中,正确的是( )
A. 在Na[Al(OH)4]溶液中,Al3+可能大量存在
B. 向Ca(ClO)2溶液中通入二氧化硫,反应的离子方程式为:
Ca2+ + 2ClO- + H2O + SO2 ═CaSO3↓+ 2HClO
C. 在由水电离出的c(OH-)=1×10-12mol·L-1的溶液中,Al3+不可能大量存在
D. 室温下pH=6的酸性溶液中,可能存在NH3·H2O分子
查看答案和解析>>
科目:高中化学 来源:2013届南京学大教育专修学校高二暑期结业测试理科化学试卷(解析版) 题型:实验题
某学生设计如下实验装置利用氯气与潮湿的消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
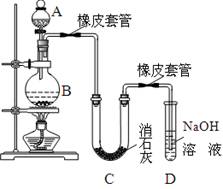
(1)A仪器的名称是 ,所盛试剂是 。
(2)漂白粉将在U型管中产生,其化学反应方程式是 。
(3)有同学建议在两个橡皮套管内的玻璃管口应尽量紧靠,原因是 。
(4)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现主要原因是在U型管中存在两个副反应:温度较高时氯气与消石灰反应生成了Ca(ClO3)2,为避免此副反应的发生,可采取的措施是 。
查看答案和解析>>
科目:高中化学 来源:2014届浙江省高一下学期期中考试文科化学试卷(解析版) 题型:选择题
已知下列氧化剂均能氧化+4价的硫元素,为除去稀硫酸中混有的亚硫酸,以得到纯净的稀硫酸,应选用的最合理的氧化剂是
A.KMnO4 B.Ca(ClO)2 C.H2O2 D.Cl2
查看答案和解析>>
科目:高中化学 来源:2010年辽宁省高三上学期10月月考(化学) 题型:选择题
(12分)某学生设计如下实验装置利用氯气与消石灰反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
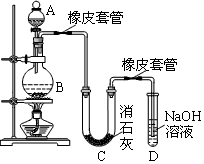
(1)A仪器的名称是 ,所盛试剂是 。
(2)漂白粉将在U型管中产生,其化学反应方程式是 。
(3)有同学建议在两个橡皮套管内的玻璃管口应尽量紧靠,原因是 。
(4)此实验结果所得Ca(ClO)2产率太低。经分析并查阅资料发现主要原因是在U型管中存在两个副反应:①温度较高时氯气与消石灰反应生成了Ca(ClO3)2,此副反应的化学方程式为: ,为避免此副反应的发生,可采取的措施是 。
②写出另一个副反应的化学方程式 。为避免此副反应发生,可采取的措施是 。
(5)在空气中,漂白粉会失效,原因是(用方程式表示) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com