
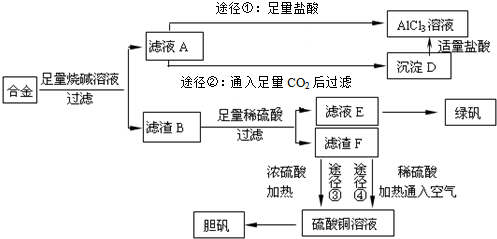
���� ����Al��Fe��Cu�ĺϽ��������NaOH��Һ�ܽ⣬ֻ��Al��NaOH��Ӧ����NaAlO2��H2����������BΪFe��Cu����B�м���ϡ���ᣬFe��Ӧ����FeSO4��Cu����Ӧ�����˵õ�����FΪCu����ҺE�к����������������ᣬ����ҺE����һϵ�в����õ��̷���
Cu��Ũ���ᷴӦ����CuSO4��Cu��������ϡ���ᷴӦҲ����CuSO4��������ͭ��Һ����һϵ�в����õ�������
��ҺA�к���NaAlO2��NaOH��;���٣�����ҺA�м���ϡ��������AlCl3��ͬʱ����NaCl��
;���ڣ�ͨ������������̼�����ɳ���DΪAl��OH��3ͬʱ����NaHCO3����Al��OH��3������ϡ�����ܽ�õ��Ȼ�����Һ��
��1���Ͻ���Al���ռ���Һ��Ӧ����ƫ�����ƺ�������
��2������FΪCu��;���������ж����������ɣ�;������û���������������ɣ�
��3��Ũ������лӷ��ԣ��������ɵĶ�����̼�к���HCl��HCl�ܺ�����������Ӧ�����Ȼ�����ˮ��
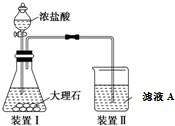
Ϊ�˱������D���٣�Ӧ����װ��I��װ��II֮������һ��װ������HCl�Ҳ��ܲ��������������ʣ�
��4������Һ����ȡ�����������Ũ������ȴ�ᾧ�����ˡ�����ķ�����
���������£�Cu�ܱ�������������ͭ���ӣ�ͬʱ����ˮ��
��5����ϵ����غ����������ĵ�CuSO4�����ʵ���֮�ȣ�
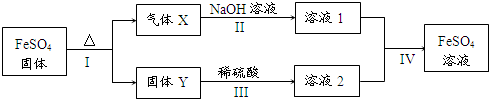
��6��a�������������ȷֽ⣬��������X��Xͨ��Ʒ����Һ����Һ��ɫ��SO2��ͨ��BaCl2��Һ��������ɫ������SO3��
b��Y����ɫ�Ļ�������Ԫ���غ�ֵY��Fe2O3��
X��NaOH��Ӧ���������ơ��������ƣ�Y��ϡ���ᷴӦ���������������������������Ʒ�Ӧ��������������
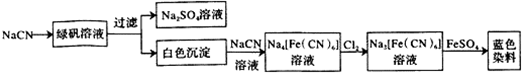
����Һ2�н����������������ӣ���KSCN��Һ���������ӣ�
����Һ1 ����Һ2 �������������Ӿ��л�ԭ�ԣ������Ӿ��������Է���������ԭ��Ӧ��������������Һ�������ƣ�
��� �⣺����Al��Fe��Cu�ĺϽ��������NaOH��Һ�ܽ⣬ֻ��Al��NaOH��Ӧ����NaAlO2��H2����������BΪFe��Cu����B�м���ϡ���ᣬFe��Ӧ����FeSO4��Cu����Ӧ�����˵õ�����FΪCu����ҺE�к����������������ᣬ����ҺE����һϵ�в����õ��̷���Cu��Ũ���ᷴӦ����CuSO4��Cu��������ϡ���ᷴӦҲ����CuSO4��������ͭ��Һ����һϵ�в����õ�������
��ҺA�к���NaAlO2��NaOH��;���٣�����ҺA�м���ϡ��������AlCl3��ͬʱ����NaCl��
;���ڣ�ͨ������������̼�����ɳ���DΪAl��OH��3ͬʱ����NaHCO3����Al��OH��3������ϡ�����ܽ�õ��Ȼ�����Һ��
��1���Ͻ���Al���ռ���Һ��Ӧ����ƫ�����ƺ����������ӷ���ʽΪ2Al+2OH-+2H2O�T2AlO2��+3H2����
�ʴ�Ϊ��2Al+2OH-+2H2O�T2AlO2��+3H2����
��2������FΪCu��;���������ж����������ɣ��������ĵ�����࣬;������û���������������ɣ����ԢܱȢ۵��ŵ��Dz�����������;�������������٣�;���ܲ��������Ⱦ���������壬
�ʴ�Ϊ��������������;�������������٣�;���ܲ��������Ⱦ���������壻
��3��Ũ������лӷ��ԣ��������ɵĶ�����̼�к���HCl��HCl�ܺ�����������Ӧ�����Ȼ�����ˮ�����²����ij����٣����ӷ���ʽΪAl��OH��3+3H+�TAl3++3H2O��
Ϊ�˱������D���٣�Ӧ����װ��I��װ��II֮������һ��װ������HCl�Ҳ��ܲ��������������ʣ����ñ���̼������Һ��
�ʴ�Ϊ��Al��OH��3+3H+�TAl3++3H2O������̼������Һ��
��4������Һ����ȡ�����������Ũ������ȴ�ᾧ�����ˡ�����ķ�����
���������£�Cu�ܱ�������������ͭ���ӣ�ͬʱ����ˮ�����ӷ���ʽΪ2Cu+O2+4H+�T2Cu2++2H2O��
�ʴ�Ϊ������Ũ����2Cu+O2+4H+�T2Cu2++2H2O��
��5������������İ�����1mol����Ӧ��ת�Ƶ�����20mol�����Ը��ݵ��ӵĵ�ʧ�غ��֪����Ӧ������Ҫ����ͭ��$\frac{20}{6}$mol��3=10mol�����ڷ�Ӧ����Ҫ����ͭ��20mol��$\frac{1}{2}$=10mol���������ĵ�CuSO4�����ʵ���֮��Ϊ1��1��
�ʴ�Ϊ��1��1��
��6��a�������������ȷֽ⣬��������X��Xͨ��Ʒ����Һ����Һ��ɫ��SO2��ͨ��BaCl2��Һ��������ɫ������SO3��
b��Y����ɫ�Ļ�������Ԫ���غ�ֵY��Fe2O3��
X��NaOH��Ӧ���������ơ��������ƣ�Y��ϡ���ᷴӦ���������������������������Ʒ�Ӧ��������������
����Һ2�н����������������ӣ���KSCN��Һ���������ӣ�����鷽��Ϊ��ȡ������Һ2���Թ��У��μӼ���KSCN��Һ����Һ��죬��֤��ԭ��Һ�к���Fe3+��
�ʴ�Ϊ��ȡ������Һ2���Թ��У��μӼ���KSCN��Һ����Һ��죬��֤��ԭ��Һ�к���Fe3+��
�ڷ�Ӧ��Ϊ2FeSO4$\frac{\underline{\;����\;}}{\;}$Fe2O3+SO2��+SO3��������ӦI�õ�16g����YΪFe2O3��Ϊ0.1mol������������X������XΪSO2��SO3���ɷ���ʽ֪���Ǹ�Ϊ0.1mol��ǡ�ñ�0.4L 1mol/L NaOH��Һ��ȫ���գ�NaOHΪ0.4mol����SO2��SO3ǡ�÷�Ӧ��2NaOH+SO2�TNa2SO3+H2O��2NaOH+SO3�TNa2SO4+H2O���ɷ���ʽ֪����Na2SO3��Na2SO4��Ϊ0.1mol����ӦIV��ΪNa2SO3��Fe2��SO4��3��Һ����������ԭ��Ӧ�����������������ӷ���ʽΪSO32-+2Fe3++H2O�TSO42-+2Fe2++2H+��
�ʴ�Ϊ��SO32-+2Fe3++H2O�TSO42-+2Fe2++2H+��
���� ���⿼����ۺϣ��漰�����Ʊ��������ƶϡ����Ӽ����֪ʶ�㣬��ȷԪ�ػ��������ʡ�����������ɫ������֮���ת������ѧʵ��ԭ����֪ʶ���ǽⱾ��ؼ���ע��ʵ��������Է������֪�������Ӽ��鷽���������ؿ���ѧ��֪ʶ�����Ӧ�ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1�� | B�� | 2�� | C�� | 3�� | D�� | 4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ�䣨min�� ���ʵ�����mol�� | 0 | 10 | 20 | 30 | 40 | 50 |
| B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
| D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
| E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
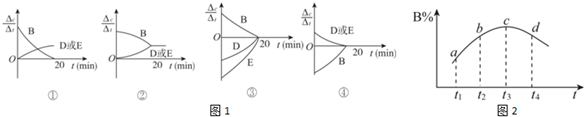
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
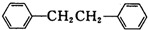 ����һ����Ҫ���л��ϳ��м��壬ʵ���ҿ��ñ���1��2һ�������飨ClCH2CH2Cl��Ϊԭ�ϣ�����ˮAlCl3���¼����Ƶã�����ȡ����Ϊ��
����һ����Ҫ���л��ϳ��м��壬ʵ���ҿ��ñ���1��2һ�������飨ClCH2CH2Cl��Ϊԭ�ϣ�����ˮAlCl3���¼����Ƶã�����ȡ����Ϊ��
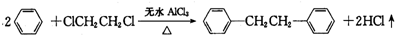
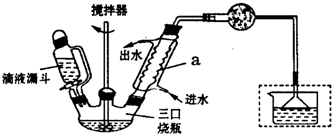
| ���� | ��Է������� | �ܶ�/��g•cm-3�� | �۵�/�� | �е�/�� | �ܽ��� |
| �� | 78 | 0.88 | 5.5 | 80.1 | ����ˮ�������Ҵ� |
| 1��2-���Ȼ��� | 99 | 1.27 | -35.3 | 83.5 | ����ˮ�����ܱ� |
| ��ˮ�Ȼ��� | 133.5 | 2.44 | 190 | 178�������� | ��ˮ�ֽ⣬�ܱ� |
| ���� | 182 | 0.98 | 52 | 284 | ����ˮ�����ܱ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
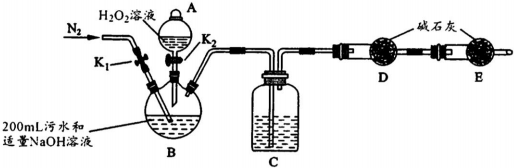
| ����1 | �ر�K1����K2����������H2O2��Һ����B���ȣ���ַ�Ӧ��ֹͣ���ȣ� |
| ����2 | ��ȴ����ע��������Bװ�õĽ���ע��ϡH2S04��Һ�� |
| ����3 | ��K1��ͨ��N2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���¶Ȳ��䣬�������������С��ԭ����һ�룬��ʱA��Ũ��Ϊԭ����2.1������m+n��p+q | |
| B�� | ��ƽ��ʱ��A��B��ת������ȣ�˵����Ӧ��ʼʱ��A��B�����ʵ���֮��Ϊm��n | |
| C�� | ��m+n=p+q����������a mol�����ƽ����ϵ���ټ���a mol��B���ﵽ��ƽ��ʱ������������ʵ�������2a | |
| D�� | ���¶Ȳ���ʱ��ѹǿ����ԭ����2�����ﵽ��ƽ��ʱ�������һ����ԭ����$\frac{1}{2}$ҪС |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H2����H1����H4����H3 | B�� | ��H1����H2����H4����H3 | C�� | ��H1����H2����H3����H4 | D�� | ��H2����H1����H3����H4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1L pH=l��������Һ�к��е�H+��ĿΪ0.2NA | |
| B�� | 1 mol�ǻ���l mol����������������������Ϊ9NA | |
| C�� | 14 g��N2��CO��ɵĻ�������к��е�ԭ����ĿΪ2NA | |
| D�� | ��״���£�2.24 L Cl2����ˮ��ת�Ƶĵ�����ĿΪ0.1NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com