
【题目】下列属于酸的是
A. HNO3 B. CaCO3 C. CO2 D. NaOH
科目:高中化学 来源: 题型:
【题目】1-萘酚用于制染料和香料等,也用于其他有机合成。下面是以1-萘酚为原料合成治疗心脏病的药物“心得安”的路线(具体反应条件和部分试剂略)。
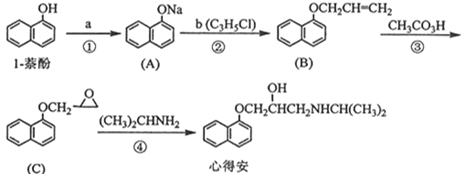
回答下列问题:
(1)试剂b中官能团的名称是_______。③的反应类型是_______。
(2)由丙烷经三步反应制备试剂b的合成路线:
![]()
反应1的试剂与条件为_______,反应2的化学方程式为________,反应3的反应类型是__________。
(3)芳香化合物D是1-萘酚的同分异构体,其分子中有两个官能团,能发生银镜反应,D能被KMnO4酸性溶液氧化成E( C2H4O2) 和芳香化合物F (C8H6O4),E和F与碳酸氢钠溶液反应均能放出CO2气体,F芳环上的一硝化产物只有一种。E的核磁共振氢谱峰面积比为______;名称是_____;D的结构简式为__________;由F生成一硝化产物的化学方程式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、(1)在Fe(OH)3胶体中逐渐滴入HI稀溶液,会出现一系列变化。
①先出现红褐色沉淀,原因是_________________________________________。
②随后沉淀溶解,溶液呈黄色,此反应的离子方程式是________________________。
③最后溶液颜色加深,此反应的离子方程式是________________________________。
(2)若用稀盐酸代替HI稀溶液,能出现(1)中所述变化现象中的____(填写上面各题序号)。
Ⅱ、某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2―→O2。
(1)该反应中,发生还原反应的过程是____________―→______________。
(2)写出该反应的化学方程式,并标出电子转移的方向和数目。
__________________________________________________________。
(3)如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温恒容时,NO2和N2O4之间发生反应,X、Y的物质的量随时间的变化如图所示。

(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间变化的曲线。
(2)若升高温度,则v正 (填“增大”或“减小”,下同),v逆 。
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3 mol·L-1·min-1,乙中v(N2O4)=0.2 mol·L-1·min-1,则 (填“甲”或“乙”)容器中反应更快。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2(g)+Cl2(g)=2HCl(g)的反应热(△H)等于-183kJ/mol ,又知H—H键的键能为436kJ/mol,Cl—Cl键的键能为243kJ/mol,则H—Cl键的键能为 ( )
A.248kJ/molB.431kJ/molC.862kJ/molD.496kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知AJ 10种物质的转化关系如图所示:
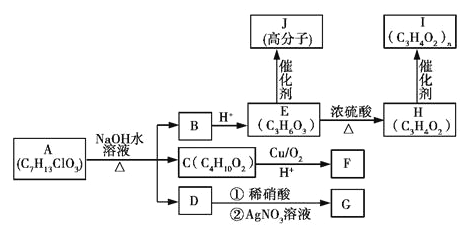
已知:①E分子中含有一个连有4个不同原子或原子团的碳原子。
②C分子中核磁共振氢谱中显示有四种不同的氢原子,且峰面积之比为4∶3∶2∶1。
③1 mol F与足量的新制氢氧化铜在加热条件下充分反应可生成2 mol砖红色沉淀。
④G为白色沉淀。
请回答下列问题:
(1)A中含有的含氧官能团的名称是______________。
(2)B的结构简式为__________________________。
(3)E生成H的化学方程式为_______________________________________。
(4)D的化学名称是__________________________________。
(5)高分子化合物J的结构简式为_______________________________。
(6)与C具有相同的官能团和相同的官能团数目,且官能团不在同一个碳原子上的C的同分异构体共有__________种,其中核磁共振氢谱有三种不同化学环境的氢原子,且峰面积之比为2∶2∶1的是________________________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应2Al+6HCl=2AlCl3+3H2中:
(1)该反应被氧化的元素是______,被还原的元素是_______(填元素符号)。
(2)该反应中氧化剂是________,还原剂是________(填元素符号)。
(3)若反应中转移电子3mol,则在反应中消耗Al________mol。
(4)用双线桥法表示下列反应的电子转移情况:________。
Zn + 2HCl = ZnCl2+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)砷及其化合物有毒,如砒霜(As2O3)有剧毒,环境监测和法医学分析砒霜中毒的反应原理:As2O3+6Zn+12HCl=6ZnCl2+2AsH3↑+3H2O。
①反应中还原剂是______________,(用化学式回答)若参加反应Zn的质量为19.5g,则生成的气体在标准状况下的体积为_________L。
②用双线桥法标出上述反应中电子转移的方向和数目____________。
(2)某同学用含少量硫酸铁的硫酸钠固体,制取芒硝(Na2SO4·10H2O),操作流程图如下所示,请回答下列问题:

①操作III所需的玻璃仪器有__________。操作V的步骤依次是______(用编号填入)
a.过滤 b.冷却、结晶 c.蒸发浓缩 d.蒸发至接近蒸干
②试剂A为_______;试剂B为______,实验中加入适量试剂B的实验方法为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠是一种高效氧化剂、漂白剂,主要用于棉纺、亚麻、纸浆等漂白。亚氯酸钠(NaClO2)在溶液中可生成C1O2、HC1O2、C1O2-、Cl-等,其中HC1O2和C1O2都具有漂白作用,但C1O2是有毒气体。经测定,25℃时各组分含量随pH变化情况如图所示(C1-没有画出)。则下列分析不正确的是( )

A. 亚氯酸钠在碱性条件下较稳定
B. 25℃时,HClO2的电离平衡常数的数值Ka=10-6
C. 25℃时,同浓度的HC1O2溶液和NaClO2溶液等体积混合,混合溶液中有c(HC1O2) +2c (H+)=c(C1O2-)+2c(OH-)
D. 使用该漂白剂的最佳pH为3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com