
【题目】表 列出了A~R十种元素在周期表的位置:
主族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | E | R | F | |||||
3 | A | C | D | H | I | G | ||
4 | B |
(1)在所示十种元素中,最活泼的金属元素是 . (均填元素符号)
(2)在所示十种元素中,原子半径最小的是 , 原子半径最大的是.(均填元素符号)
(3)C元素在周期表中的位置: .
(4)写出EF2分子的电子式 .
(5)H,I,G三种元素的氧化物对应的水化物中酸性由大到小的顺序排列为 . (填化学式).
(6)写出G的单质与A的最高价氧化物对应水化物反应的离子方程式 .
(7)E单质和R的最高价氧化物对应水化物相互反应的化学方程式 .
【答案】
(1)K
(2)O;O
(3)第三周期IIA族
(4)![]()
(5)HClO4>H2SO4>H2SiO3
(6)Cl2+2OH﹣=Cl﹣+ClO﹣+H2O
(7)C+4HNO3(浓) ![]() ?4NO2↑+CO2↑+2 H2O
?4NO2↑+CO2↑+2 H2O
【解析】解:由元素在周期表中的位置可知,A为Na,B为钾,C为Mg,D为Al,E为碳,H为Si,R为氮,F为氧,I为硫,G为Cl.(1)同周期自左而右金属性减弱,同主族自上而下金属性增强,故上述元素中最活泼的金属元素是K,所以答案是:K;(2)同周期自左而右原子半径减小,同主族自上而下原子半径增大,一般电子层越多原子半径越大,上述元素中,原子半径最小的是O,原子半径最大的是K,所以答案是:O;K;(3)由C的位置可知,处于周期表中第三周期IIA族,所以答案是:第三周期IIA族;(4)EF2为CO2 , 分子中C原子与氧原子之间形成2对共用电子对,电子式为 ![]() ,所以答案是:
,所以答案是: ![]() ;(5)同周期自左而右非金属性增强,非金属性越强,最高价氧化物对应水化物的酸性越强,故酸性:HClO4>H2SO4>H2SiO3 , 所以答案是:HClO4>H2SO4>H2SiO3;(6)氯气与氢氧化钠反应生成氯化钠、次氯酸钠与水,反应离子方程式为:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O,所以答案是:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;(7)碳与浓硝酸反应生成二氧化碳、二氧化氮与水,反应方程式为:C+4HNO3(浓)
;(5)同周期自左而右非金属性增强,非金属性越强,最高价氧化物对应水化物的酸性越强,故酸性:HClO4>H2SO4>H2SiO3 , 所以答案是:HClO4>H2SO4>H2SiO3;(6)氯气与氢氧化钠反应生成氯化钠、次氯酸钠与水,反应离子方程式为:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O,所以答案是:Cl2+2OH﹣=Cl﹣+ClO﹣+H2O;(7)碳与浓硝酸反应生成二氧化碳、二氧化氮与水,反应方程式为:C+4HNO3(浓) ![]() 4NO2↑+CO2↑+2 H2O, 所以答案是:C+4HNO3(浓)
4NO2↑+CO2↑+2 H2O, 所以答案是:C+4HNO3(浓) ![]() 4NO2↑+CO2↑+2 H2O.
4NO2↑+CO2↑+2 H2O.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图: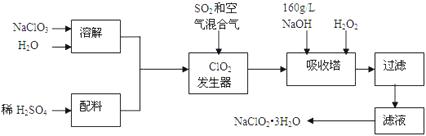
已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出产品NaClO23H2O;
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
(1)发生器中发生反应的离子方程式为。发生器中鼓入空气的作用可能是。
a.将SO2氧化成SO3 , 增强酸性 b.将NaClO3还原为ClO2 c.稀释ClO2以防止爆炸
(2)吸收塔内发生反应的化学方程式为;吸收塔内的温度不能超过20℃,其目的是。
(3)吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。以下还可以选择的还原剂是(选填序号)。
a.Na2O2 b.Na2S c.FeCl2
(4)从滤液中得到NaClO2·3H2O粗晶体的实验操作依次是。
(5)某学习小组用碘量法测定粗产品中亚氯酸钠的含量,实验如下:
a.准确称取所得亚氯酸钠样品m g于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应,将所得混合液配成250 ml待测溶液。(已知:ClO2-+4I-+4H+=2H2O+2I2+Cl-)
b.移取25.00 ml待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1 Na2S2O3标准液滴定至终点,重复2次,测得平均值为V ml 。(已知:I2+2S2O32-=2I-+S4O62-)
①达到滴定终点时的现象为 。
②该样品中NaClO2的质量分数为 (用含m、c、V的代数式表示,结果化成最简。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的A、B、C三种物质(都是气体)放入固定体积为10L的密闭容器中,一定条件下发生反应,一段时间内测得各物质的量变化如图所示. 请解答下列问题: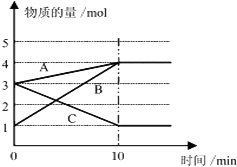
(1)反应的化学方程式用A,B,C可表示为 .
(2)用B的浓度变化表示在0~10min内的反应速率是 .
(3)在该条件达到反应的限度(平衡状态)时反应物的转化率(转化率═转化的物质的量/初始物质的量×100%,计算结果保留1位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,可形成氢氧燃料电池.通常氢氧燃料电池有酸式(当电解质溶液为硫酸时)和碱式[当电解质溶液为NaOH(aq)或KOH(aq)时]两种.试回答下列问题: 
(1)酸式电池的电极反应:负极 , 正极;电池总反应:;电解质溶液pH的变化(填“变大”“变小”或“不变”).
(2)碱式电池的电极反应:负极 , 正极;电池总反应:;电解质溶液pH的变化(填“变大”“变小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合物X由Na2O,Fe2O3、Cu、SiO2中的一种或几种物质组成.某兴趣小组以两条途径分别对X进行如下实验探究.下列有关说法不正确的是( ) 
A.无法判断混合物中是否含有Na2O
B.由Ⅱ可知X中一定存在SiO2
C.1.92g固体成分为Cu
D.15.6g混合物X中m(Fe2O3):m(Cu)=1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食盐(NaCl)是生活中常用的调味品,HCl是胃酸的主要成分,下列关于两种物质的说法正确的是( )
A.炒菜时放入食盐并不破坏NaCl中的化学键
B.HCl的电子式是 ![]()
C.NaCl熔化时破坏共价键
D.HCl的结构式是H﹣Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不可能是原电池反应的是( )
A.Fe+2H+=Fe2++H2↑
B.H++OH﹣=H2O
C.2H2+O2=2H2O
D.Fe2++Zn=Fe+Cu2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com