
| A. | 用新制Cu(0H)2悬浊液不能鉴别麦芽糖和蔗糖 | |
| B. | 硫酸铵和醋酸铅溶液均可使鸡蛋清溶液中的蛋白质变性 | |
| C. | 油是不饱和高级脂肪酸的简单甘油酯,是纯净物 | |
| D. | 用银镜反应可证明蔗糖是否转化为葡萄糖,但不能证明是否完全转化 |
分析 A.麦芽糖属于还原性糖,蔗糖不是还原性糖;
B.硫酸铵能使蛋白质发生盐析,重金属盐能使蛋白质变性;
C.油是不饱和高级脂肪酸的甘油酯,属于混合物;
D.葡萄糖中含有醛基,具有醛的性质.
解答 解:A.麦芽糖含有醛基,蔗糖没有醛基,含有醛基的物质与新制Cu(OH)2悬浊液反应会生成砖红色沉淀,所以用新制Cu(OH)2悬浊液可鉴别麦芽糖和蔗糖,故错误;
B.硫酸铵能使蛋白质发生盐析,重金属盐能使蛋白质变性,所以硫酸铵不能使蛋白质变性,故B错误;
C.油是不饱和高级脂肪酸的甘油酯,属于混合物,故C错误;
D.葡萄糖中含有醛基,具有醛的性质,能发生银镜反应,故D正确;
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及物质或官能团检验等知识点,明确官能团或物质性质是解本题关键,注意盐析和变性的区别,题目难度不大.


科目:高中化学 来源: 题型:选择题

| A. | 滤液A中的阳离子为Fe2+、Fe3、H+ | B. | 样品中金属Fe的质量为4.48g | ||
| C. | 样品中CuO的质量为4.0 | D. | V=448 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (1)(2)(3)(4)(5) | B. | (4)(5)(7)) | C. | (4)(5) | D. | (3)(4)(5)(7) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 达到化学反应限度时,可生成2mol NH3 | |
| B. | 向容器中再加入N2,可以加快反应速率 | |
| C. | 降低温度可以加快反应速率 | |
| D. | 1mol N2 和3mol H2的总能量低于2mol NH3的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水溶性:乙醇>新戊烷>苯酚 | |
| B. | 同质量的物质燃烧消耗O2量:乙烷>甲烷>乙炔 | |
| C. | 密度:水>苯>硝基苯 | |
| D. | 沸点:正戊烷>异戊烷>新戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
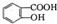 与适量NaHC03溶液反应制备
与适量NaHC03溶液反应制备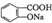
| A. | 只有①③④ | B. | 只有①③ | C. | 只有② | D. | 都不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com