
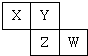
| A. | 元素X是自然界中形成化合物种类最多的元素 | |
| B. | 气态氢化物的稳定性Z>W>Y | |
| C. | 原子半径由大到小排列顺序Z>Y>X | |
| D. | W只有一种氧化物 |
分析 短周期元素中,若W原子最外层电子数是其内层电子总数的$\frac{3}{5}$,结合位置可知,W在第三周期,则最外层电子数为6,质子数为16,即W为S,由X、Y、Z、W在元素周期表中的位置可知,Z为P,Y为N,X为C,然后结合元素周期律及元素化合物知识来解答.
解答 解:短周期元素中,若W原子最外层电子数是其内层电子总数的$\frac{3}{5}$,结合位置可知,W在第三周期,则最外层电子数为6,质子数为16,即W为S,由X、Y、Z、W在元素周期表中的位置可知,Z为P,Y为N,X为C,
A.X为C,可形成有机物化合物,C是自然界中形成化合物种类最多的元素,故A正确;
B.非金属性越强,氢化物越稳定,则气态氢化物的稳定性W>Z,Y>Z,故B错误;
C.电子层越多,原子半径越大,同周期原子序数大的原子半径小,则原子半径由大到小排列顺序Z>X>Y,故C错误;
D.W有二氧化硫、三氧化硫两种氧化物,故D错误;
故选A.
点评 本题考查位置、结构、性质的关系,为高频考点,把握元素的位置、原子结构推断元素为解答的关键,侧重分析与推断能力的考查,注意元素周期律及元素化合物知识的应用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 该溶液中,H+、Al3+、Cl?能大量共存 | |
| B. | 溶液中c(H2CO3)<c(CO32?) | |
| C. | 该溶液中阳离子总数大于阴离子总数 | |
| D. | 常温下,加水稀释,$\frac{c({H}^{+}).c(C{O}_{3}^{2-})}{c(HC{O}_{3}^{-})}$变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | |||
| Y | Z | W | A |
| T | B |
| A. | X、W、Z元素的原子半径与它们的气态氢化物的热稳定性变化趋势相反 | |
| B. | Y、Z、B、W、A元素性质均较为活泼,但其中的某些元素在自然界中仍可以游离态的形式存在,它们的最高价氧化物的水化物的酸性依次递增 | |
| C. | 工业上电解A的钠盐溶液可以得到多种产物,为防止产物互相反应常使用阴离子交换膜 | |
| D. | 根据元素周期律,可以推测T元素的单质具有半导体特性,T2X3具有氧化性和还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .W、X、Y的离子半径由大到小的顺序为S2->O2->Al3+(用离子符号回答)
.W、X、Y的离子半径由大到小的顺序为S2->O2->Al3+(用离子符号回答)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
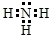 ;由A、D两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X中所含化学键类型极性键、非极性键;(填写“极性共价键”、“非极性共价键”、“离子键”)向X中加入酸性KMnO4溶液,写出二者恰好反应的离子方程式5H2O2+2MnO4-+6H+=5O2↑+2Mn2++8H2O;
;由A、D两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X中所含化学键类型极性键、非极性键;(填写“极性共价键”、“非极性共价键”、“离子键”)向X中加入酸性KMnO4溶液,写出二者恰好反应的离子方程式5H2O2+2MnO4-+6H+=5O2↑+2Mn2++8H2O;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
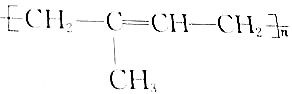
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 成语 | 化学原理 | |
| A | 炉火纯青 | 通过观察火焰的颜色来判断炉内的温度 |
| B | 火树银花 | 发生了焰色反应 |
| C | 百炼成钢 | 通过多次锻炼,使生铁中碳等杂质因挥发而降低达到了钢的标准 |
| D | 青出于蓝而胜于蓝 | 蓝色的靛蓝燃料发生化学反应生成一种深蓝色的新燃料 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | cB=$\frac{ν_B}{ν_A}$•$\frac{{{c_A}{V_A}}}{V_B}$ | B. | cB=$\frac{ν_B}{ν_A}$•$\frac{{{c_A}{V_B}}}{V_A}$ | ||
| C. | cB=$\frac{{{c_A}{V_A}}}{V_B}$ | D. | cB=$\frac{ν_A}{ν_B}$•$\frac{{{c_A}{V_A}}}{V_B}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1 mol Cl2与过量的镁反应,转移 2NA个电子 | |
| B. | 常温常压下,16 g CH4含有 10NA个电子 | |
| C. | 1 mol•L -1 Na2SO4溶液中含有 NA个SO42- | |
| D. | 常温常压下,22.4 L CO2含有N A个CO2分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com