
【题目】向浓度相等、体积均为50 mL的A、B两份NaOH溶液中,分别通入一定量的CO2后,再稀释到100 mL。
(1)在NaOH溶液中通入一定量的CO2后,溶液中溶质的组成可能是①________,②________,③________,④________。

(2)在稀释后的溶液中逐滴加入0.1 mol ·L-1的盐酸,产生CO2的体积(标准状况)与所加盐酸的体积关系如图所示。
①A曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2的最大体积是________mL(标准状况)。
②B曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为______________________。
③原NaOH溶液的物质的量浓度为_____________________________。
【答案】 NaOH、Na2CO3 Na2CO3 Na2CO3、NaHCO3 NaHCO3 112 NaOH、Na2CO3 0.150 mol·L-1
【解析】(1)由CO2+2NaOH═Na2CO3+H2O、CO2+NaOH═NaHCO3,二氧化碳少量时固体为①Na2CO3和NaOH;以1:2恰好反应时为②Na2CO3;物质的量比介于1:1~1:2之间为③Na2CO3和NaHCO3;二氧化碳过量时为④NaHCO3,故答案为:Na2CO3和NaOH;Na2CO3;Na2CO3和NaHCO3;NaHCO3;(2)由图可知,对应B溶液来说,滴加盐酸60mL时没有气体生成,可能发生OH-+H+=H2O和CO32-+H+=HCO3-,假设原溶液中只有碳酸钠,生成碳酸氢钠需要盐酸的体积和碳酸氢钠生成氯化钠需要盐酸的体积相等,实际上需要盐酸的体积60mL远远大于碳酸氢钠生成氯化钠需要盐酸的体积(75-60)mL=15mL,说明原溶液中的溶质是NaOH和Na2CO3;对于A溶液来说,滴加盐酸25mL时没有气体生成,可能发生OH-+H+=H2O和CO32-+H+=HCO3-,假设原溶液中只有碳酸钠,生成碳酸氢钠需要盐酸的体积和碳酸氢钠生成氯化钠需要盐酸的体积相等,实际上需要盐酸的体积25mL小于碳酸氢钠生成氯化钠需要盐酸的体积(75-25)mL=50mL,说明原溶液中的溶质是Na2CO3和NaHCO3,①对于A溶液来说,滴加盐酸25mL时有气体生成,逐滴加入0.1molL-1 的盐酸,当生成CO2气体时,发生反应HCO3-+H+=H2O+CO2↑
则HCO3-+H+=H2O+CO2↑,n(CO2)=0.05L×0.1mol/L=0.005mol,标况下体积为0.005mol×22.4L/mol=0.112L=112mL,故答案为:112;②由上述分析可知,B中溶质是Na2CO3和NaOH,由消耗盐酸的关系可知,物质的量比为3:1,故答案为:Na2CO3和NaOH;
③加入足量的盐酸后的溶液中均只存在NaCl,n(HCl)=n(NaOH)=0.075L×0.1mol/L=0.0075mol,c(NaOH)=![]() ==0.15mol/L。
==0.15mol/L。


科目:高中化学 来源: 题型:
【题目】下列有关有机物的说法中正确的是( )
A.凡是含碳元素的化合物都属于有机物
B.易溶于汽油、酒精、苯等有机溶剂中的物质,一定是有机物
C.所有的有机物都很容易燃烧
D.大多数有机物的熔沸点比较低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(EGC)的结构如下图所示。关于EGC的下列叙述中正确的是

A. 分子中所有的原子共面
B. 1mol EGC与4mol NaOH恰好完全反应
C. 易发生氧化反应和取代反应,难发生加成反应
D. 遇FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国每年产生的废旧铅蓄电池约330万吨。从含铅废料(PbSO4、PbO2、PbO等)中回收铅,实现铅的再生,意义重大。一种回收铅的工作流程如下:

(1)铅蓄电池放电时,PbO2作____极。
(2)过程I,已知:PbSO4、PbCO3的溶解度(20℃)见图l;Na2SO4、Na2CO3的溶解度见图2。

①根据图l写出过程I的离子方程式:__________。
②生产过程中的温度应保持在40℃,若温度降低,PbSO4的转化速率下降。根据图2,解释可能原因:
i.温度降低,反应速率降低; ii.____(请你提出一种合理解释)。
③若生产过程中温度低于40℃,所得固体中,含有较多Na2SO4杂质,原因是____。
(3)过程Ⅱ,发生反应2PbO2+H2C2O4=2PbO+H2O2+2CO2↑。实验中检测到有大量O2放出,推测PbO2氧化了H2O2,通过实验证实了这一推测。实验方案是____。
(已知:PbO2为棕黑色固体;PbO为橙黄色固体)
(4)过程Ⅲ,将PbO粗品溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的电解液,电解Na2PbCl4溶液,生成Pb,如图3。
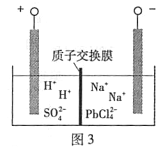
①阴极的电极反应式是____________。
②电解一段时间后,PbCl2'浓度极大下降,为了恢复其浓度且实现物质的循环利用,阴极区采取的方法是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属及其合金的说法不正确的是
A. 目前我国流通的硬币是由合金材料制造的
B. 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用
C. 镁在空气中燃烧发出耀眼的白光,可用于制作照明弹
D. 生铁、普通钢和不锈钢中的碳含量依次增加
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的离子,能在溶液中大量共存的是
A. Na+、Cu2+、Cl-、SO42- B. Ca2+、Na+、NO3-、CO32-
C. H+、Na+、Cl-、CO32- D. K+、H+、S042-、0H-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中关于物质的性质和用途的说法均正确且有因果关系的是
选项 | 性质 | 用途 |
A | 溴化银有感光性 | 用于变色玻璃 |
B | 新制氯水显酸性 | 漂白有色布条 |
C | 浓硫酸有强氧化性 | 干燥剂 |
D | 氨气是碱性气体 | 液氨作制冷剂 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1.5molH2SO4的质量是_____,其中含有___mol 氢原子。
(2)9.03×1023个氨分子含___mol氨分子,___mol氢原子,___个电子。
(3)含有6.02×1023个OH-的Ca(OH)2的物质的量是____,质量是____。
(4)已知16gA和20gB恰好完全反应生成0.04molC和31.76gD,则C的摩尔质量为____。
(5)在同温同压下,相等质量的氧气和臭氧,它们的物质的量之比为____,原子个数比为____。
(6)Fe(OH)3胶体的制备__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com