
用右图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是( )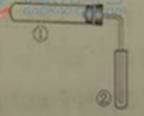
| ①中实验 | ②中现象 | |
| A | 铁粉与水蒸气加热 | 肥皂水冒泡 |
| B | 加热NH4Cl和Ca(OH)2混合物 | 酚酞溶液变红 |
| C | NaHCO3 | 澄清石灰水变浑浊 |
| D | 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
A是一种有机合成中间体,其结构简式为
A的合成路线如下图,其中B~H分别代表一种有机物。

请回答下列问题:
(1)A中碳原子的杂化轨道类型有 ① ;A的名称(系统命名)是 ② ;第⑧步反应的类型是 ③ 。
(2)第①步反应的化学方程式是
(3)C物质与CH2=C(CH3)COOH按物质的量之式1:1反应,其产物经加聚得到 可作隐形眼镜的镜片材料I。I的结构简式是
(4)第⑥步反应的化学方程式是
(5)写出含有六元环,且一氯代物只有两种(不考虑立体异构)的A的同分异构体的结构简式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
合成氨是人类科学技术上的一项重大突破,其反应原理为:
N2(g)+3H2(g)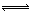 2NH3(g) ∆H=—92.4kJ•mol‾1
2NH3(g) ∆H=—92.4kJ•mol‾1
一种工业合成氨的简易流程图如下:

(1)天然气中的H2S杂质常用常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式: 。
(2)步骤II中制氯气原理如下:

对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的是 。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
利用反应②,将CO进一步转化,可提高H2产量。若1mol CO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18mol CO、CO2和H2的混合气体,则CO转化率为 。
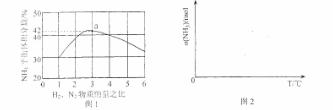
(3)图1表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数: 。
(4)依据温度对合成氨反应的影响,在图2坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图。
(5)上述流程图中,使合成氨放出的热量得到充分利用的主要步骤是(填序号) ,简述本流程中提高合成氨原料总转化率的方法: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式错误的是
A.向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++ SO42 - =BaS04↓+2H2O
B.酸性介质中KMnO4氧化 H2O2:2MnO4- +5H2O2+6H+ = 2Mn2++5O2↑+ 8H2O
C.等物质的量的MgCl2、Ba(OH)2 和 HC1 溶液混合:Mg2++2OH-= Mg(OH)2↓
D.铅酸蓄电池充电时的正极反应:PbSO4 + 2H2O-2e- = PbO2+4H++SO42 -
查看答案和解析>>
科目:高中化学 来源: 题型:
用FeCl3酸性溶液脱除H2S后的废液,通过控制电压电解得以再生。某同学使用石墨电极,在不同电压(x)下电解pH=1的0.1mol/LFeCl2溶液,研究废液再生机理。记录如下(a、b、c代表电压值:)

(1)用KSCN溶液检验出Fe3+的现象是_______。
(2)I中,Fe2+产生的原因可能是Cl-在阳极放电,生成的Cl2将Fe2+氧化。写出有关反应的方程式__________________________。
(3)由II推测,Fe3+产生的原因还可能是Fe2+在阳极放电,原因是Fe2+具有_____性。
(4)II中虽未检测出Cl2,但Cl-在阳极是否放电仍需进一步验证。电解pH=1的NaCl溶液做对照实验,记录如下:
| 序号 | 电压/V | 阳极现象 | 检验阳极产物 |
| IV | a>x≥c | 无明显变化 | 有Cl2 |
| V | c>x≥b | 无明显变化 | 无Cl2 |
①NaCl溶液的浓度是________mol/L。
②IV中检测Cl2的实验方法:____________________。
③与II对比,得出的结论(写出两点):___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
答案 (1)③④⑤⑥⑦⑧⑨ (2)B>A>C
解析 (1)元素原子得电子能力的强弱与元素氢化物的溶解性无关,所以①不符合题意;氢化物的酸性强弱和元素原子得电子能力大小没有固定的对应关系,所以②也不符合题意,其他均符合题意。(2)由金属B的最高价氧化物的水化物的碱性比A的最高价氧化物的水化物的碱性强,可判断失电子能力B>A;又根据A与C形成原电池,C作正极,可判断失电子能力A>C,故三种金属元素的原子失电子能力B>A>C。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知33As、35Br位于同一周期。下列关系正确的是 ( )
A.原子半径:As>Cl>P
B.热稳定性:HCl>AsH3>HBr
C.还原性:As3->S2->Cl-
D.酸性:H3AsO4>H2SO4>H3PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
(I)X、Y、Z、A、L、E六种短周期主族元素的原子序数依次增大,其中X、E的单质在常温下呈气态,E在常温下是黄绿色气体;Y的原子的最外层电子数是其电子层数的2倍,Z在同周期的主族元素中原子半径最大,A是地壳中含量最多的金属元素,L的单质晶体熔点高、硬度大,是一种重要的半导体材料。
用化学用语回答下列问题:
(1)L的元素符号为 ;A在元素周期表中的位置为
(2)Y、L、E的最高价含氧酸的酸性由弱到强的顺序是
(3)Y的最高价氧化物的电子式为 。
(II)下列物质A~F是我们熟悉的单质或化合物,其中A、E均为(I)中元素形成的单质,B是常见的金属,且B的合金用量最大;在适当的条件下,它们之间可以发生如下图所示的转化。

试回答下列问题:
(1)B的化学式是 ;
(2)反应F D的化学方程式 。
D的化学方程式 。
(3)检验F中金属阳离子的常用方法是 。
(4)写出C与过量氨水反应的离子方程式是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com