
| A. | 1.2×10-5 mol•L-1 | B. | 2.4×10-4 mol•L-1 | ||
| C. | 3.6×10-4 mol•L-1 | D. | 4.8×10-4 mol•L-1 |
分析 根据沉淀溶解平衡CrO42-+Ba2+?BaCrO4及Ksp(BaCrO4)=c(CrO42-)×c(Ba2+)=1.2×10-10,可得c(Ba2+),然后结合废水中CrO42-浓度小于5.0×10-7mol•L-1进行计算.
解答 解:BaCrO4 ?CrO42-+Ba2+
5.0×10-7mol•L-1 c(Ba2+)
则:Ksp(BaCrO4)=c(CrO42-)×c(Ba2+)=5.0×10-7×c(Ba2+)=1.2×10-10,
解得:c(Ba2+)=2.4×10-4mol/L,即:若使废水中CrO42-浓度达标,Ba2+的浓度应不小于2.4×10-4mol/L,
故选B.
点评 本题考查了难溶物溶解平衡及其计算,题目难度中等,明确难溶物溶度积常数的概念及表达式为解答关键,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
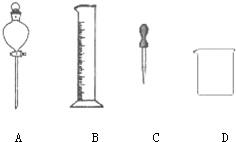
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、SiO32-、Cl- | B. | H+、NH4+、Al3+、SO42- | ||
| C. | Na+、CO32-、SO32- SO42- | D. | Na+、S2-、OH-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.8 g 2H2O所含中子总数为NA | |
| B. | 1 L 1 mol/L的甲醇水溶液中含有氢原子总数为4NA | |
| C. | 12g石墨和C60的混合物中质子总数为6NA | |
| D. | 反应KIO3+6HI═KI+3H2O+3I2中,生成1mol I2转移电子的总数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 | |
| B. | 凡质子数相同的微粒,其化学性质一定相同 | |
| C. | 含氧酸可作氧化剂,无氧酸只作还原剂 | |
| D. | 元素的非金属性越强,其简单阴离子的还原性越弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
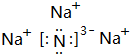 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素位于元素周期表第三周期表ⅢB族 | |
| B. | 该元素位于s区 | |
| C. | 该元素为金属元素 | |
| D. | 该元素原子M能层共有8个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com