
| A. | NaCl Na+${\;}_{•}^{•}$$\underset{\stackrel{••}{CI}}{••}$${\;}_{•}^{•}$ | B. | H2S H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{S}}{••}$${\;}_{•}^{•}$]2-H+ | ||
| C. | N2 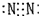 | D. | NH4I 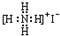 |
分析 A.氯化钠为离子化合物,氯离子核外电子没有标出;
B.硫化氢是H和S构成的共价化合物;
C.氮气分子中存在氮氮三键,氮原子最外层为8电子;
D.碘化铵是离子化合物,由氨根离子与碘离子构成.
解答 解:A.氯化钠为离子化合物,氯离子带电荷并需用方括号括起来,钠离子用离子符号表示,电子式: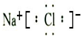 ,故A错误;
,故A错误;
B.硫化氢是共价化合物,不存在离子键,硫原子与氢原子间形成1对共用电子对,电子式为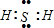 ,故B错误;
,故B错误;
C.氮气分子中存在氮氮三键,氮原子最外层为8电子,N2的电子式为: ,故C正确;
,故C正确;
D.碘化铵是离子化合物,由氨根离子与碘离子构成,电子式为: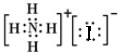 ,故D错误,
,故D错误,
故选C.
点评 本题考查电子式的判断,难度不大,要明确用电子式表示离子化合物、共价化合物、阴离子及单质分子的方法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 混合气体中一定含有乙烯 | |
| B. | 混合气体中一定含有甲烷 | |
| C. | 混合气体中一定含有乙炔 | |
| D. | 混合气体一定是由烷烃和烯烃构成的混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
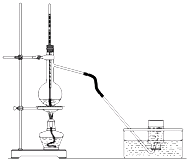 实验室制取乙烯的装置如图所示,请回答:
实验室制取乙烯的装置如图所示,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 该反应为放热反应 | B. | 该反应为吸热反应 | ||
| C. | 断裂H-H键吸收能量 | D. | 生成H-O键放出能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2.4g金属镁所含电子数目为0.2NA | |
| B. | 1 mol CH4所含质子数目为10NA | |
| C. | 标准状况下22.4 L H2O所含分子数目为NA | |
| D. | 18g NH4+所含电子数目为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
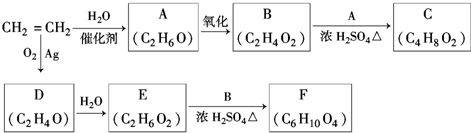
 ,该反应的类型为酯化反应;
,该反应的类型为酯化反应;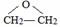 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 0.1 | 0.5 | 1 | 10 | |
| 400 | 99.2% | 99.6% | 99.7% | 99.9% |
| 500 | 93.5% | 96.9% | 97.8% | 99.3% |
| 600 | 73.7% | 85.8% | 89.5% | 96.4% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/LNa2CO3溶液中:2c(Na+)=c(HCO3-)+c(H2CO3)+c(C032-) | |
| B. | 向0.1mol/L氯化铵溶液中滴加浓盐酸可能有c(NH4+)=c(H+) | |
| C. | pH=4的醋酸与pH=10的NaOH溶液等体积混合后pH>7 | |
| D. | 将0.2mol/LNaA溶液和某浓度的盐酸等体积混合所得中性溶液中:c(Na+)=c(A-)+c(Cl-)=0.2mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com