
����Ŀ��ijС��ͬѧͨ��ʵ���о�FeCl3��Һ��Cu�۷�����������ԭ��Ӧ��ʵ���¼���£�
��� | I | II | III |
ʵ�鲽�� |
�������2mL����ˮ |
���������2mL����ˮ |
���������2mL����ˮ |
ʵ������ | ͭ����ʧ����Һ��ɫ��dz����������ˮ������������ | ͭ����ʣ�࣬��Һ��ɫ��ȥ����������ˮ�����ɰ�ɫ���� | ͭ����ʣ�࣬��Һ��ɫ��ȥ�� �����ɫ����������ˮ���ް�ɫ���� |
����˵������ȷ���ǣ� ��
A.ʵ��I��II��III�о������˷�Ӧ2Fe3++Cu=2Fe2++Cu2+
B.�Ա�ʵ��I��II��III˵����ɫ�����IJ���������ͭ�۵�������Һ�������������й�
C.ʵ��I��III�м�������ˮ��c(Cu2+)��ͬ
D.��ʵ��III��Ӧ�����Һ�м��뱥��NaCl��Һ���ܳ��ְ�ɫ����
���𰸡�C
��������
A������ʵ������Һ�о�����Fe3+��������ͭ�ۣ����ᷢ��2Fe3++Cu=2Fe2++Cu2+����A��ȷ��
B���Ա�ʵ��I������֪����ɫ�����IJ�����ͭ�۵����йأ��Ա�ʵ������III��֪����ɫ�����IJ�������Һ�������������йأ���B��ȷ��
C��ʵ��I��ͭ������������ȫ��ʧ�����Բ���ȷ���Ƿ�Fe3+ȫ����Ӧ������ʵ��I��III�м�������ˮ��c(Cu2+)��һ����ͬ����C����
D������ʵ�����������֪����ͭ�����������Ӵ���ʱ�����������������ʵ������Ӧ�����Һ�м��뱥��NaCl��Һ�����ܳ��ְ�ɫ��������D��ȷ��
�ʴ�ΪC��


 �����Ļ���������人������ϵ�д�
�����Ļ���������人������ϵ�д� ���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д�
���������ּ���ÿһ��ȫ�º�����ҵ��ϵ�д� ��ٽ������½������������ϵ�д�
��ٽ������½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������װ�û��������ʵ�飬���ܴﵽĿ�ĵ��ǣ� ��
|
|
|
���ڹ����� |
A.��ϡ������Cu��Ӧ��ȡNO | B.��֤������ԭ��Ӧ���е���ת�� | C.������Ȫʵ�� | D.��֤����������ܷ�����Ӧ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��װ��(��)��һ�ֿɳ���ص�ʾ��ͼ��װ��(��)Ϊ���ص�ʾ��ͼ��װ��(��)�����ӽ���Ĥֻ����![]() ͨ������طŵ�Ļ�ѧ����ʽΪ
ͨ������طŵ�Ļ�ѧ����ʽΪ![]() �����պ�Kʱ��X��������Һ�ȱ��ɫ������˵����ȷ���ǣ� ��
�����պ�Kʱ��X��������Һ�ȱ��ɫ������˵����ȷ���ǣ� ��
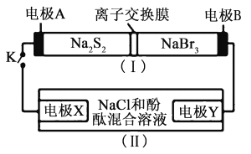
A.װ��(��)��AΪ����
B.�缫X�ĵ缫��Һ����ԭ��![]()
C.�ŵ�ʱ���缫B�ĵ缫��ӦʽΪ![]()
D.��ԭ��س��ʱ![]() ��������ͨ�����ӽ���Ĥ
��������ͨ�����ӽ���Ĥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���йؾ������������ȷ���ǣ� ��
A����SiO2�����У���Si��O���ɵ���С��Ԫ���й���8��ԭ��
B����28g������У���Si��Si���ۼ�����Ϊ4NA
C�����ʯ���۷е���ھ���裬����ΪC��C������С��Si��Si��
D��þ�ͺ�ͭ�ͽ����������λ����Ϊ12
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2019��ŵ������ѧ���������ӵ������ѧ�ҵ���Ҫ����֮һ���з����˵缫����������������ﮣ�LiFePO4����LiFePO4��һ���Ʊ�������ͼ��
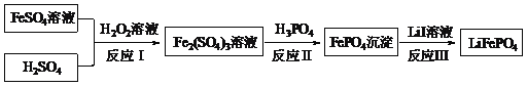
����˵����ȷ���ǣ� ��
A.��������ĵ���ʽΪ��![]()
B.��Ӧ������ӷ���ʽΪ��2Fe2++H2O2=2Fe3++2OH-
C.��Ӧ������ӷ���ʽΪ��Fe3++PO![]() =FePO4��
=FePO4��
D.��Ӧ��Ļ�ѧ���̿���Ϊ��2FePO4��2LiI=2LiFePO4��I2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й��ڱ���������ȷ����
A.���ķ���ʽΪC6H6��������ʹ����KMnO4��Һ��ɫ�����ڱ�����
B.�ӱ��Ľṹ��ʽ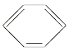 �����������к���̼̼˫����Ӧ����ϩ��
�����������к���̼̼˫����Ӧ����ϩ��
C.�ڴ��������£�����Һ�巴Ӧ�����屽�������˼ӳɷ�Ӧ
D.������Ϊƽ���������νṹ��6��̼ԭ��֮��Ļ�ѧ����ȫ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��˫��ˮ��һ����Ҫ����������Ư����������������˫��ˮ���������������䷴Ӧԭ��������������ͼ��ʾ��
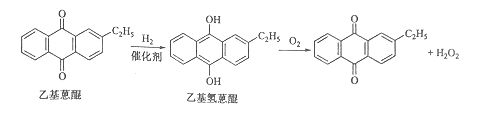
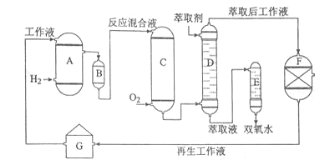
A���⻯�� B�������� C�������� D����ȡ�� E.�������� F������Һ����װ�� G������Һ����װ��
���������У����һ����������л��ܼ����Ƴɹ���Һ����һ�����¶ȡ�ѹ���ʹ��������½����⻯���پ���������ȡ�������ȹ��յõ�˫��ˮ���ش��������⣺
��1���������Ʊ�˫��ˮ���������ĵ�ԭ����_______��ѭ��ʹ�õ�ԭ����______�����ƹ���Һʱ�����л��ܼ���������ˮ��ԭ����______��
��2���⻯��A�з�Ӧ�Ļ�ѧ����ʽΪ_______������������C�ķ�Ӧ���Һ�е���Ҫ����Ϊ_______��
��3����ȡ��D�е���ȡ����____��ѡ��������ȡ����ԭ����______��
��4������Һ����װ��F��Ҫ����������H2O2��ԭ����______��
��5��˫��ˮŨ�ȿ���������������KMnO4��Һ�ⶨ���÷�Ӧ�����ӷ���ʽΪ_______��һ��˫��ˮ����������Ϊ27.5%�����ܶ�Ϊ1.10g��cm3������Ũ��Ϊ______mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ʾ��װ���У���ƿ�г�����������a�����ι��е�Һ��b������ƿ�ڣ���������ƿ��Ȼ����ɼ�f���ձ��е�Һ��d����Ȫ״��������ռ���������ƿ����a��b�ֱ���(����)
ѡ�� | a(��������) | b(Һ��) |
|
A | NO2 | ˮ | |
B | CO2 | ����NaHCO3��Һ | |
C | Cl2 | ����NaCl��Һ | |
D | NH3 | 1 mol��L��1���� |
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ᣨCCl3COOH��������ˮ�г�����Ⱦ�����ֱ���������⡣ͨ��Fe/Cu��ط��ͷҶٷ��ɽ����������ȥ��
��1��pH=4ʱ���������������ˮ����Ͷ����м��ͭм��ͨ��ԭ��ط�Ӧ���ɵĻ�����ԭ�ӣ�H����CCl3COOH���Ⱥ�ת��ΪCHCl2COOH��
��ԭ��ط�Ӧʱ�ĸ�����ӦʽΪ___��
��д��������ԭ�ӣ�H����CCl3COOH��Ӧ�����ӷ���ʽ��___��
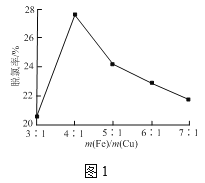
����м��ͭм��������һ�����ı���м��ͭм�������ȣ�ˮ���е�λʱ�������������������ͼ1��ʾ����m(Fe)/m(Cu)����4ʱ����м����Խ��������Խ�͵�ԭ����___��
��2��ȡ������Ӧ�����Һ�������м���H2O2������ͼ2��ʾת���������ǻ����ɻ�����OH������OH�ܽ���Һ�е�CHCl2COOH�����ʽ�һ�����ȳ�ȥ��
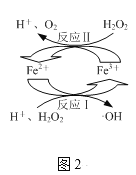
��ͼ2��ʾת���л��ϼ�δ�����仯��Ԫ����___��
��д��ͼ2��ʾת���з�Ӧ������ӷ���ʽ��___��
�ۿ���ˮ����pH��ͬ��������������ͼ3��ʾ����pH��4�����������½���ԭ����___��

�ܼ���H2O2���������Һ���¶ȣ��¶ȹ���ʱ�����ʼ�С��ԭ����___��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com