
| A. | O2 | B. | NO2 | C. | NO | D. | SO2 |
分析 排空气法适合收集密度与空气密度相差较大且和空气中的成分不反应的气体,若密度比空气的大,采用向上排空气法,若密度比空气的小,采用向下排空气法,密度与空气密度接近的不能用排气法收集.不能用排空气法只能用排水法收集说明该气体能和空气中的成分反应,和水不反应,据此分析解答.
解答 解:A.氧气密度大于空气密度,为空气中的主要成分之一,可以用向上排空气法收集,故A不选;
B.二氧化氮和水反应生成硝酸和一氧化氮,所以不能用排水集气法收集,故B不选;
C.一氧化氮不稳定,能与空气中的氧气反应生成二氧化氮,且密度与空气密度接近,不能用排气法收集,故C选;
D.二氧化硫和水反应,所以不能用排水集气法收集,故D不选;
故选C.
点评 本题考查了气体的收集方法,难度不大,明确气体的性质是解本题的关键,知道气体的收集常用方法有排水法和排空气法,根据气体的性质选取相应的收集方法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
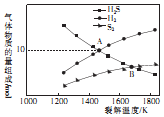 硫化氢是天然气及石油中的含硫杂质,近年来发现H2S可用于高效制取氢气.
硫化氢是天然气及石油中的含硫杂质,近年来发现H2S可用于高效制取氢气.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 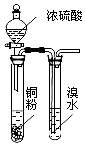 用图所示装置验证浓硫酸具有强氧化性 | |
| B. | 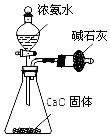 用图所示装罝制取干燥的 NH3 | |
| C. | 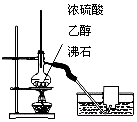 用图所示装置制取并收集乙烯 | |
| D. | 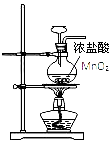 用图所示装置制取 Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W与其他四种元素形成的二元化合物中其化合价均为+1 | |
| B. | X与Y形成的化合物溶于水后溶液呈碱性 | |
| C. | 最高价氧化物的水化物的酸性:M>Z | |
| D. | 简单离子半径:W<Y<X<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 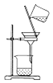 用装置分离Fe(OH)3胶体和NaCl溶液 | |
| B. | 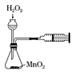 用装置定量测定H2O2的分解速率 | |
| C. |  用装置将CuSO4•5H2O变无水CuSO4 | |
| D. | 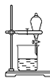 用装置④分离饱和Na2CO3溶液和CH3COOCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | B. | 2KClO3$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+3O2↑ | ||
| C. | 3Mg+Fe2O3═3MgO+2Fe | D. | Al+Fe2O3═Al2O3+Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 木材纤维和土豆淀粉遇碘水均显蓝色 | |
| B. | 食用花生油和鸡蛋清都能发生水解反应 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | 煤是混合物,含有大量的芳香烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com