
下列离子方程式正确的是
A.用铜作电极电解CuSO4溶液:2Cu2++2H2O电解2Cu+4H++O2↑
B.硅酸钠溶液与醋酸溶液混合:SiO32-+H+=H2SiO3↓
C.H2O2溶液中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O
D. Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源:2013-2014天津市第二学期期中检测高一化学试卷(解析版) 题型:选择题
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是

A.非金属性:Z<T<X B.R与Q的电子数相差26
C.气态氢化物稳定性:R <T<Q D.最高价氧化物的水化物的酸性:T>Q
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市下学期期中考试高二化学试卷(解析版) 题型:选择题
下列醇中既能发生消去反应,又能被氧化为酮的是

A.①④⑤ B . ②④⑥  C . ② ⑥ D . ①②⑥
C . ② ⑥ D . ①②⑥
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市南开区高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
利用下表提供的实验器材(规格和数量不跟)能完成相应实验的是
选项 | 实验器材(省略夹持装置) | 相应实验 |
A | 烧杯、玻璃棒、短颈玻璃漏斗 | 苯甲酸的重结晶 |
B | 烧杯、玻璃棒、胶头滴管、分液漏斗 | 用溴水和CCl4除去NaBr溶液中少量NaI |
C | 烧杯、玻璃棒、胶头滴管、容量瓶 | 用固体NaCl配制0.5 mol/L NaCl溶液 |
D | 烧杯、玻璃棒、胶头滴管 | 用盐酸除去BaSO4中少量BaCO3 |
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市南开区高三二模试卷理综化学试卷(解析版) 题型:实验题
(18分)甲、乙两个研究性学习小组为测定氨分子中氮、氢原子个数比,设计了如下实验流程:
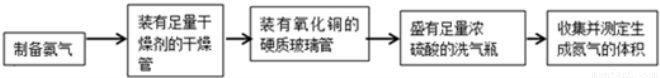
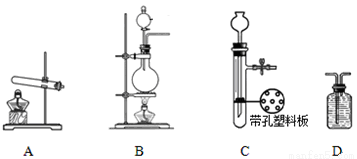
实验中,先用制得的氨气排尽洗气瓶前所有装置中的空气,再连接洗气瓶和气体收集装 置,立即加热氧化铜。反应完成后,黑色氧化铜转化为红色的铜。下图A、B、C为甲、乙两小组制取氨气时可能用到的装置,D为盛有浓硫酸的洗气瓶。
甲小组测得:反应前氧化铜的质量m1 g、氧化铜反应后剩余固体的质量m2g、生成氮气在标准状况下的体积V1L。乙小组测得:洗气前装置D的质量m3g、洗气后装置D的质量为m4g、生成氮气在标准状况下的体积V2L。请回答下列问题:
(1)检查A装置气密性的操作是____________________________________________________。
(2)实验室检验氨气的操作和现象是____________________________________。
(3)甲、乙两小组选择了不同的方法制取氨气,请将实验装置的字母编号和制备制备原理填写在下表的空格中。
| 实验装置 | 实验药品 | 制备原理 |
甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为____________ |
乙小组 | _____ | 浓氨水、氢氧化钠 | 用化学平衡原理分析氢氧化钠的作用:_______ |
(4)甲小组用所测数据计算出氨分子中氮、氢的原子个数之比为________________。
(5)乙小组用所测数据计算出氨分子中氮、氢的原子个数之比明显小于理论值,其原因是_______。为此,乙小组在原有实验的基础上增加了一个装有某药晶的实验仪器,重新实验。根据实验前后该药品的质量变化及生成氮气的体积,得出了合理的实验结果。该药品的名称是________。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市高三毕业班联考二理综化学试卷(解析版) 题型:实验题
(18分)实验室测定碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数w(Na2CO3),称取此混合物5.0g,溶于水中,配成250mL溶液。
方案一:沉淀法。利用化学反应把HCO3-、CO32-完全转化为沉淀,称量干燥沉淀的质量,由此计算混合物中w (Na2CO3)。
(1)量取100 mL配制好的溶液于烧杯中,滴加足量沉淀剂,把溶液中HCO3-、CO32-完全转化为沉淀,应选用的试剂是___________ (填编号)。
A.CaCl2溶液 B.MgSO4溶液 C.NaCl溶液 D.Ba(OH)2溶液
(2) 简述证明HCO3-、CO32-已完全沉淀的实验操作_________________________。
(3) 过滤,提取沉淀,则过滤操作所需要的玻璃仪器除烧杯外,还有________________________。
(4) 将沉淀洗涤,并充分干燥,称量沉淀的质量为mg,由此可以计算w(Na2CO3)。如果此步中,沉淀未干燥充分就称量,则测得w (Na2CO3)________________(填偏大或偏小、无影响)。
方案二:量气法。量取10.00mL配制好的溶液与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01×105Pa)的体积,由此计算混合物中w (Na2CO3)。
(1) 装置中导管a的作用是 。
(2) 反应结束后,为了准确地测量气体体积,量气管在读数时应注意:
①_______________________________,
②_________________________________,
③眼睛视线与液面最低处相平。
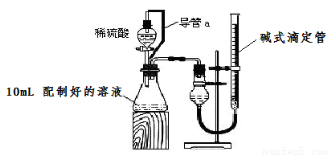
(3)实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL。则 产生CO2的体积为 mL。
方案三:滴定法。量取25.00 mL配制好的溶液加入锥形瓶中,滴加2滴酚酞试剂,摇匀,用0.2000 mol/L盐酸进行滴定到终点(已知终点时反应H++CO32- =HCO3-恰好完全)。重复此操作2次,消耗盐酸的体积平均值为20.00 mL。
(1)量取25.00 mL配制好的溶液,应选择_______________仪器来完成。
(2)判断滴定终点的依据是_____________________。
(3)此法测得w(Na2CO3)= %。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市高三毕业班联考二理综化学试卷(解析版) 题型:选择题
下列有关说法不正确的是
A.实验室制取氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液
B.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解
C.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,则水电离的热化学方程式为:H2O(l) H+(aq)+OH-(aq) ΔH= +57.3 kJ·mol-1
H+(aq)+OH-(aq) ΔH= +57.3 kJ·mol-1
D.生铁发生吸氧腐蚀和析氢腐蚀的负极反应均为:Fe-2e- =Fe2+
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市东丽区第一学期期末质量监测高一年级化学试卷(解析版) 题型:选择题
下列有关物质存放方法错误的是
A.金属钠存放于煤油中
B.漂白粉长期放置在烧杯中
C.铝片长期放置在不密封的纸盒里
D.FeSO4溶液存放在加有少量铁粉的试剂瓶中
查看答案和解析>>
科目:高中化学 来源:2013-2014天津五区县高一下学期期末考试化学试卷(解析版) 题型:选择题
在炼铜的过程中发生:Cu2S + 2Cu2O = 6Cu + SO2↑,则下列叙述正确的是
A.该反应从电子转移角度看,与SO2 + 2H2S = 3S + 2H2O是同一反应类型
B.该反应从电子转移角度看,每生成6 mol铜,转移电子12 mol
C.该反应中,氧元素氧化了硫元素
D.该反应中,Cu2S既是还原剂又是氧化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com