
| 1 |
| 2 |
0.4c×
| ||
| 0.6c |
| 2 |
| 3 |
| 0.2c |
| 2 |
| 3 |
| 0.2c |
| ||
| ||


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:
| A、3.0L0.1mol?L-1 NaOH溶液中缓慢通入CO2至溶液增重8.8 g时,溶液中:c(Na+)>c(CO32->c(HCO3-)>c(OH-)>c(H+) |
| B、常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7:c(Na+)>c(CH3COO-)>c(Cl-)=c(CH3COOH)>c(H+)=c(OH-) |
| C、常温下,pH=6的NaHSO3溶液中:c(SO32-)-c(H2SO3)=9.9×10-7 mol?L-1 |
| D、物质的量浓度之比为1:2的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=2c(HCO3-)+2c(H2CO3)+2c(CO32-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 碱 | 酸 | 盐 | 酸性氧化物 | |
| A | 纯碱 | HNO3 | NaHCO3 | SO2 |
| B | 烧碱 | H2SO4 | NaCl | CO |
| C | 苛性钠 | CH3COOH | 石灰石 | 水 |
| D | 熟石灰 | H2CO3 | 纯碱 | SO3 |
| A、A | B、B | C、C | D、D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
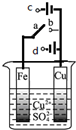
| A、开关a和b相连时,溶液中SO42-移向Cu极 |
| B、开关a和c相连时,保护Fe极不被腐蚀则为外加电流阴极保护法 |
| C、无论开关a和c或开关a和b相连,Fe电极反应方程式:Fe-2e?=Fe2? |
| D、开关a和d相连时,形成电解池,溶液从蓝色逐渐变成浅绿色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
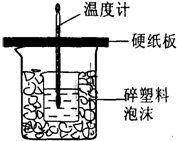 中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:
中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量.某学生想通过测定反应过程中所放出的热量来计算中和热.他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
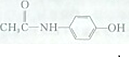 是最常用的非甾体消炎解热镇痛药,F用如下路线来合成
是最常用的非甾体消炎解热镇痛药,F用如下路线来合成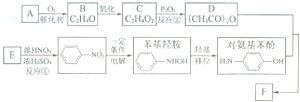
 ,下列关于W的说法正确的是( )
,下列关于W的说法正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发:利用物质颗粒的大小 |
| B、萃取:利用物质的溶解度不同 |
| C、过滤:利用物质的沸点不同 |
| D、蒸馏:利用物质的沸点不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com