
下列有关化学用语或名称,表达正确的是( )
A. 聚丙烯的结构简式为: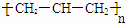 B. 苯分子的比例模型:
B. 苯分子的比例模型:
C. 四氯化碳分子的电子式为: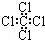 D. 乙烯的结构简式:CH2CH2
D. 乙烯的结构简式:CH2CH2
考点: 结构简式;电子式;球棍模型与比例模型.
分析: A.聚丙烯的主链只有2个C;
B.比例模型主要体现的是组成该分子的原子间的大小关系;
C.CCl4为共价化合物,各原子满足8电子稳定结构;
D.乙烯中含有碳碳双键,官能团在结构简式中不能省略.
解答: 解:A.聚丙烯为丙烯的加聚反应产物,聚丙烯正确的结构简式为: ,故A错误;
,故A错误;
B.比例模型主要体现的是组成该分子的原子间的大小关系,碳原子半径大于氢原子,所以苯的比例模型是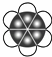 ,故B正确;
,故B正确;
C.CCl4为共价化合物,各原子满足8电子稳定结构,电子式为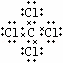 ,故C错误;
,故C错误;
D.乙烯中含有碳碳双键官能团,结构简式为CH2=CH2,故D错误,
故选B.
点评: 本题主要考查了结构简式、电子式、比例模型、高聚物分子式的判断,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列做法会对人体健康造成较大危害的是( )
A.用大量SO2漂白银耳
B.用小苏打(NaHCO3)焙制糕点
C.用食醋清洗热水瓶胆内壁附着 的水垢(CaCO3)
的水垢(CaCO3)
D.用消毒液(有效成分NaClO)对餐具进行杀菌消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
现有下列物质,用编号填空回答下列问题:
A.干冰 B.金刚石 C.氦 D.过氧化钠 E.二氧化硅 F.溴化铵
(1)通过非极性键形成的原子晶体是: .
(2)可由原子直接构成的晶体是: .
(3)含有离子键、共价键、配位键的化合物是: .
(4)含有非极性键的离子化合物是: .
(5)已知微粒间的作用力包括离子键、共价键、金属键、范德华力、氢键.氯化钠熔化,粒子间克服的作用力为 ;二氧化硅熔化,粒子间克服的作用力为 ;干冰气化,粒子间克服的作用力为 .A、B、C、D四种物质的熔点从低到高的顺序为 (填序号).
查看答案和解析>>
科目:高中化学 来源: 题型:
mA(s)+nB(g)⇌qC(g),的可逆反应,在1×105pa与2×105pa两种压力条件下,B的体积分数与温度的关系如右图所示,有关叙述正确的是( )
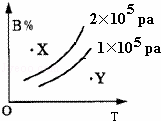
|
| A. | △H>0 | B. | X点,v正>v逆;Y点,v正<v逆 |
|
| C. | m+n>q | D. | X点比Y点反应速率快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
、TiO2可通过下述两种方法制备金属钛:
方法一:电解TiO2来获得Ti,将处理过的TiO2作阴极,石墨为阳极,熔融CaO为电解液,用石墨作电解槽池.
(1)阳极的电极反应式为 .
(2)电解过程中需定期更换石墨电极的原因是 .
方法二:先将TiO2与Cl2、C反应得到TiCl4,再用镁还原得到Ti.
(3)TiO2(s)+2Cl2(g)⇌TiCl4(l)+O2(g)△H=+151kJ•mol﹣1该反应难以发生,原因是 .
不能直接由TiO2 和Cl2反应(即氯化反应)来制取TiCl4,当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使反应在高温条件下能顺利进行.
(4)已知:C(s)+O2(g)=CO2(g)△H=﹣394kJ•mol﹣1
TiO2(s)+C(s)+2Cl2(g)=TiCl4(l)+CO2(g)△H=
(5)从化学平衡的角度解释:往氯化反应体系中加入碳时,氯化反应能顺利进行的原因 .
查看答案和解析>>
科目:高中化学 来源: 题型:
关于原子轨道的说法正确的是( )
|
| A. | 凡是中心原子采取sp3杂化方式成键的分子其几何构型都是正四面体 |
|
| B. | CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的 |
|
| C. | sp3杂化轨道是由同一个原子中能量相近的s轨道和p轨道混合起来形成的一组能量相同的新轨道 |
|
| D. | 凡AB3型的共价化合物,其中心原子A均采用sp3杂化方式成键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
|
| A. | 卤代烃在NaOH存在下水解生成的有机物都是醇 |
|
| B. | 所有的一元醇都能被氧化为具有相同碳原子数的醛或酮 |
|
| C. |
|
|
| D. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com