
(10分)工业上制备BaCl2的工艺流程图如图:
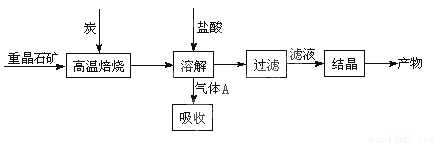
某研究小组在实验室用重晶石(主要成分BaSO4)对工业过程进行模拟实验。查资
料得:
BaSO4(s) + 4C(s) 4CO(g) + BaS(s) ΔH1 = +571.2 kJ·mol-1 ①
4CO(g) + BaS(s) ΔH1 = +571.2 kJ·mol-1 ①
BaSO4(s) + 2C(s) 2CO2(g) + BaS(s) ΔH2= +226.2 kJ·mol-1 ②
2CO2(g) + BaS(s) ΔH2= +226.2 kJ·mol-1 ②
(1)①制备BaCl2的工艺流程图中气体A用过量NaOH溶液吸收,得到硫化钠。Na2S水解的离子方程式为 。
②常温下,相同浓度的Na2S和NaHS溶液中,下列说法正确的是 (填字母)。
A.Na2S溶液的pH比NaHS溶液pH小
B.两溶液中含有的离子种类不同
C.两溶液中滴入同体积同浓度的盐酸,产生气体速率相等
D.两溶液中加入NaOH固体,c(S2-)都增大
E.NaHS溶液中:c(Na+) >c(HS-) >c(OH-) >c (H+)
(2)向BaCl2溶液中加入AgNO3和KBr,当两种沉淀共存时,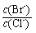 = 。 【已知:Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10】
= 。 【已知:Ksp(AgBr)=5.4×10-13,Ksp(AgCl)=2.0×10-10】
(3)反应C(s) + CO2(g) 2CO(g)的ΔH =
2CO(g)的ΔH =
(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是: (只要求答一条)。
(1)S2-+H2O HS-+OH-;D、E;(2)2.7×10-3;(3)+172.5KJ/mol;(4)炭过量使BaSO4充分还原
HS-+OH-;D、E;(2)2.7×10-3;(3)+172.5KJ/mol;(4)炭过量使BaSO4充分还原
【解析】
试题分析:(1)①BaSO4与焦炭在高温下发生反应产生BaS,BaS与盐酸发生反应:BaS+2HCl=BaCl2+H2S↑。H2S 气体被NaOH溶液吸收得到Na2S。Na2S是强碱弱酸盐,弱酸根离子水解使溶液显碱性。水解的离子方程式为S2-+H2O HS-+OH-。②A.NaHS是H2S 的一级电离产生的,Na2S是H2S 的二级电离产生的,对于多元弱酸来说,一级电离>>二级电离。溶液的酸性主要一级电离决定。根据盐的水解规律:有弱才水解,谁弱谁水解,,越弱越水解,谁强显谁性。所以溶液的碱性Na2S>NaHS。即Na2S溶液的pH比NaHS溶液pH大。错误。B.在两种物质的溶液中都含有Na+、S2-、HS-、H2S、H+、OH-。离子种类相同。错误。C.当向Na2S溶液中加入盐酸时,首先发生S2-+H+=HS-,没有气体产生;然后发生HS-+H+=H2S↑,放出气体。而向NaHS溶液中加入盐酸时立即发生HS-+H+=H2S↑,放出气体。所以两溶液中滴入同体积同浓度的盐酸,产生气体速率不相等。错误。D.当向Na2S和NaHS的溶液中分别加入NaOH溶液时由于增大了OH-离子的浓度,所以水解平衡:S2-+H2O
HS-+OH-。②A.NaHS是H2S 的一级电离产生的,Na2S是H2S 的二级电离产生的,对于多元弱酸来说,一级电离>>二级电离。溶液的酸性主要一级电离决定。根据盐的水解规律:有弱才水解,谁弱谁水解,,越弱越水解,谁强显谁性。所以溶液的碱性Na2S>NaHS。即Na2S溶液的pH比NaHS溶液pH大。错误。B.在两种物质的溶液中都含有Na+、S2-、HS-、H2S、H+、OH-。离子种类相同。错误。C.当向Na2S溶液中加入盐酸时,首先发生S2-+H+=HS-,没有气体产生;然后发生HS-+H+=H2S↑,放出气体。而向NaHS溶液中加入盐酸时立即发生HS-+H+=H2S↑,放出气体。所以两溶液中滴入同体积同浓度的盐酸,产生气体速率不相等。错误。D.当向Na2S和NaHS的溶液中分别加入NaOH溶液时由于增大了OH-离子的浓度,所以水解平衡:S2-+H2O HS-+OH-、HS-+H2O
HS-+OH-、HS-+H2O H2S+OH-逆向移动。使c(S2-)都增大。所以正确。E.NaHS=Na++ HS-; HS-发生水解反应 HS-+H2O
H2S+OH-逆向移动。使c(S2-)都增大。所以正确。E.NaHS=Na++ HS-; HS-发生水解反应 HS-+H2O H2S+OH-要消耗,所以c(Na+) >c(HS-);HS-水解消耗了水电离产生的H+,使H+的浓度减小,最终当达到水的电离平衡时c(OH-) >c (H+) 。盐的电离远大于弱电解质水的电离,所以c(HS-) >c(OH-)。因此E.NaHS溶液中:c(Na+) >c(HS-) >c(OH-) >c (H+) 。正确。(2)向BaCl2溶液中加入AgNO3和KBr,发生反应:Ag++Cl-=AgCl↓; Ag++Br-=AgBr↓.Ksp(AgBr)= C(Ag+)·C(Br-) =5.4×10-13; Ksp(AgCl)= C(Ag+)·C(Cl-)=2.0×10-10当两种沉淀共存时,C(Ag+)相同。
H2S+OH-要消耗,所以c(Na+) >c(HS-);HS-水解消耗了水电离产生的H+,使H+的浓度减小,最终当达到水的电离平衡时c(OH-) >c (H+) 。盐的电离远大于弱电解质水的电离,所以c(HS-) >c(OH-)。因此E.NaHS溶液中:c(Na+) >c(HS-) >c(OH-) >c (H+) 。正确。(2)向BaCl2溶液中加入AgNO3和KBr,发生反应:Ag++Cl-=AgCl↓; Ag++Br-=AgBr↓.Ksp(AgBr)= C(Ag+)·C(Br-) =5.4×10-13; Ksp(AgCl)= C(Ag+)·C(Cl-)=2.0×10-10当两种沉淀共存时,C(Ag+)相同。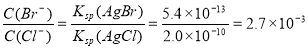 。(3) (①-②)÷2可得:反应C(s) + CO2(g)
。(3) (①-②)÷2可得:反应C(s) + CO2(g)  2CO(g)的ΔH =+172.5KJ/mol;(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是使BaSO4充分还原得到BaS。
2CO(g)的ΔH =+172.5KJ/mol;(4)实际生产中必须加入过量的炭,同时还要通入空气,其目的是使BaSO4充分还原得到BaS。
考点:考查BaSO4的用途、Na2S和NaHS溶液的比较、溶度积常数的应用及热化学方程式的书写等知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届浙江省宁波市八校高二上学期期末联考化学试卷(解析版) 题型:选择题
下列各项所给的两个量,前者—定小于后者的是:
①纯水在25℃和80℃的pH; ②1moINaHSO4和1mo1 Na2SO4在熔化状态下的离子数;
③25℃时,等体积且pH都等于3的盐酸和AlCl3的溶液中,已电离的水分子数;
④常温下,pH为10的氨水溶液和pH为12氨水溶液中所含溶质分子数。
A.①② B.②④ C.①③ D.②③
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高二下学期第一次质量检测化学试卷(解析版) 题型:选择题
已知化合物A(C4Si4H8)与立方烷(C8H8)的分子结构相似,如图:则C4Si4H8的二氯代物的同分异构体数目为( )

A.6 B.5 C.4 D.3
查看答案和解析>>
科目:高中化学 来源:2015届河南许昌市五校高二下学期第一次联考化学试卷(解析版) 题型:选择题
下列混合溶液中,各离子浓度的大小关系不正确的是( )
A.物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:
c(CH3COO-) + c(CH3COOH)=2c(Na+)
B. 0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
C. 物质的量浓度相等Na2CO3和NaHCO3溶液等体积混合,离子浓度的大小顺序是
c (Na+)>c (HCO3-)> c(CO32-)>c(OH-)> c(H+)
D.NH4Cl溶液中:c(H+) = c(NH3·H2O) +c(OH-)
查看答案和解析>>
科目:高中化学 来源:2015届河南许昌市五校高二下学期第一次联考化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.铅蓄电池放电时的负极和充电时的阳极均发生还原反应
B.燃放的焰火是某些金属元素焰色反应所呈现出的色彩,焰色反应属于化学变化
C.利用丁达尔现象可以区分氢氧化铁胶体和硫酸铜溶液
D.工业上制粗硅的主要反应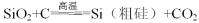
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高二上学期期末检测化学试卷(A)(解析版) 题型:选择题
下列叙述不正确的是:
A.用反应热数据的大小判断不同反应反应速率的快慢
B.用pH数据推测相同浓度的不同强酸弱碱盐在水溶液中水解程度的大小
C.应用盖斯定律,可计算某些难以直接测量的反应焓变
D.用平衡常数的大小判断化学反应可能进行的程度
查看答案和解析>>
科目:高中化学 来源:2015届河南省洛阳市高二上学期期末检测化学试卷(A)(解析版) 题型:选择题
在指定的条件下,下列各组离子一定能大量共存的是
A.无色的溶液中:Fe3+、K+、NO3-、Cl-
B.pH=13的溶液中:NH4+、Na+、SO42-、Cl-
C.含有大量Ba2+ 的溶液中:NH4+、Na+、Cl-、H+
D.c(H+)=0.1 mol·L-1的溶液中:K+、I-、Cl-、NO3-
查看答案和解析>>
科目:高中化学 来源:2015届河北省邯郸市高二上学期期末考试化学试卷(解析版) 题型:选择题
电解硫酸溶液时,放出25mL(标况)O2,若以等量的电量在同样条件下电解盐酸溶液,
所放出的气体的体积最接近下列数据中的
A.45mL B.50mL C.75mL D.100mL
查看答案和解析>>
科目:高中化学 来源:2015届河北省高二下学期第一次月考化学试卷(解析版) 题型:选择题
加拿大阿尔贡天文台在星际空间发现了HC9N链状分子,其结构式为:
HC≡C—C≡C—C≡C—C≡C—C≡N,这是人类迄今发现的最重星际有机分子,有关该分子的说法不正确的是
A.该物质属于不饱和烃
B.该分子中所有原子处在一条直线上
C.该分子在一定条件下可发生加成反应
D.该分子碳、氮原子均满足八电子结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com