
| A. | 金 | B. | 硫 | C. | 铜 | D. | 铁 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
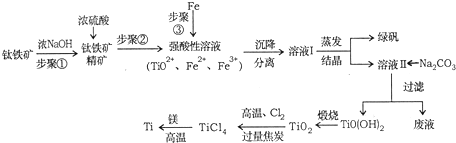
| PH | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | TiO(OH)2 |
| 开始沉淀 | 1.1 | 4.5 | 7 | 1 |
| 完全沉淀 | 2.8 | 6.4 | 9.2 | 2.7 |
| TiCl4 | Mg | MgCl2 | Ti | |
| 熔点/ | -25.0 | 648.8 | 714 | 1667 |
| 沸点/ | 136.4 | 1090 | 1412 | 3287 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
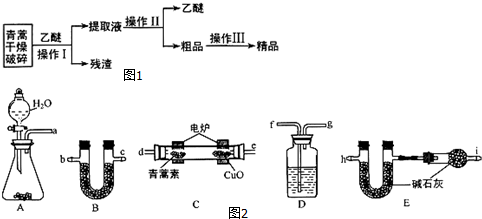
| 装置质量 | 实验前/g | 实验后/g |
| B | 22.6 | 42.4 |
| E(不含干燥管) | 80.2 | 146.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
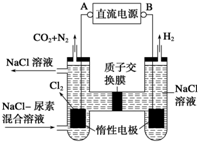
| A. | A 极为电源的负极 | |
| B. | 阳极室中发生的反应只有CO(NH2)2-6e-+6OH -=N2↑+CO2↑+5H2O | |
| C. | 阴极室溶液的 PH 电解前后保持不变 | |
| D. | 除去 3.6 克尿素时阴极一定生成 H26.72L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Z、W均可形成两种常见氧化物 | |
| B. | 四种元素在自然界均不能以游离态存在 | |
| C. | 元素X、Y、W的最高化合价均与其族序数相等 | |
| D. | 离子半径:W>Z>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
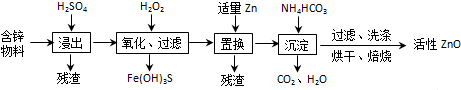
| A. | 上述流程中,浸出时用的是60% H2SO4(密度是1.5g/cm3),如配制100 mL这种H2SO4溶液,则需要18.4mol•L-1的浓硫酸约为49.9mL | |
| B. | 若生成的沉淀是形态均为Zna(OH)b (CO3)c的(a、b、c都是正整数)两种碱式碳酸锌的混合物,则分别可能是Zn5(OH)6(CO3)2 与Zn3(OH)6CO3 | |
| C. | 若加入NH4HCO3后生成的沉淀是Zn5(OH)6(CO3)2,则该反应为5ZnSO4+10NH4HCO3═Zn5(OH)6(CO3)2↓+5(NH4)2SO4+8CO2↑+2H2O | |
| D. | 加入氧化剂H2O2后,只有Fe(OH)3沉淀出现,若溶液中c(Fe3+)═2.6×10-15mol•L-1,则溶液中c(Cu2+)≤2.2×10-4mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体样品于试管中,滴加足量1mol•L-1 H2SO4溶液,然后将内壁附有澄清石灰水的烧杯罩于试管口 | 若澄清石灰水未见浑浊,则假设1成立;若澄清石灰水变浑浊,则假设2或假设3成立 或假设1不成立. |
| 步骤2: | |
| 步骤3: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
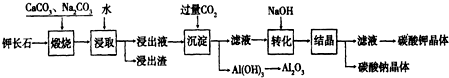
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=7的溶液不一定是中性溶液 | |
| B. | 0.2 mol•L-1的盐酸与等体积水混合后pH=1(体积变化忽略不计) | |
| C. | 能自发进行的化学反应,一定是△H<0、△S>0 | |
| D. | NaNO2固体溶于水会促进水的电离(已知Ka(HNO2)=4.6×10-4) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com