
| A. | 亚硫酸 | B. | 氢硫酸 | C. | 碳酸钠溶液 | D. | 氢氧化钠溶液 |
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 非金属性比硫强 | B. | 最高价氧化物的化学式是SeO2 | ||
| C. | 酸性:H2SeO4>H2SO4 | D. | 气态氢化物的化学式为H2Se |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
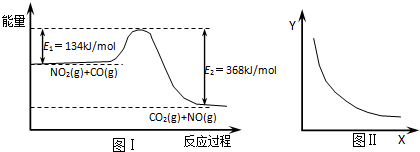
| A. | 该反应的焓变△H=234kJ/mol | |
| B. | 若X表示CO的起始浓度,则Y表示的可能是NO2的转化率 | |
| C. | 若X表示反应时间,则Y表示的可能是混合气体的密度 | |
| D. | 若X表示温度,则Y表示的可能是CO2的物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①或② | B. | 只有②或④ | C. | 只有①或②或③ | D. | ①②③④中任意一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取少量试液,加入用盐酸酸化的氯化钡溶液,有白色沉淀生成 | |
| B. | 取少量试液,加入氯化钡溶液,有白色沉淀生成,再加稀硝酸沉淀不消失 | |
| C. | 取少量试液,加入硝酸钡溶液,有白色沉淀生成 | |
| D. | 取少量试液,加入盐酸无现象,再加氯化钡溶液,有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在金属元素与非金属元素的分界线附近可以寻找制备半导体材料的元素 | |
| B. | 在过渡元素中可以寻找制备催化剂及耐高温和耐腐蚀的元素 | |
| C. | 在非金属元素区域可以寻找制备新型农药材料的元素 | |
| D. | 最外层电子数为8的粒子是稀有气体元素的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大多数化学反应在一定条件下都有一定的限度 | |
| B. | 化学反应在一定条件下达到限度时,正、逆反应速率都等于零 | |
| C. | 当某反应体系中气体压强不在改变时,该反应一定达到了反应限度 | |
| D. | 当某反应在一定条件下达到反应限度时,反应物和生成物的浓度一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
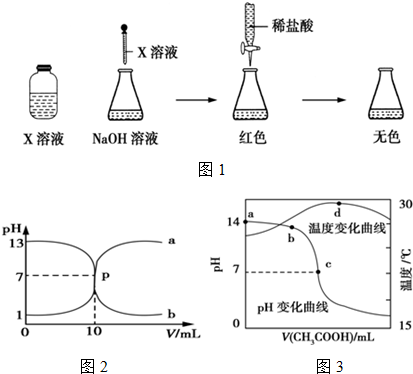
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com