
| A. | H2SO4→HCl→K2S→NaOH→CO2 | B. | NaCl→Na2SO4→Na2S→NH3•H2O→HCl | ||
| C. | Na2S→Na2SO4→NaCl→NaOH→HCl | D. | NaCl→Na2SO4→H2S→NaOH→CO2 |
分析 氯离子只能使银离子转化为沉淀,硫酸根离子只能使钡离子转化为沉淀,硫化氢只能使铜离子转化为沉淀,过量NaOH只能使镁离子转化为沉淀,滤液中通入足量二氧化碳可使偏铝酸根离子转化为沉淀,以此来解答.
解答 解:氯离子只能使银离子转化为沉淀,硫酸根离子只能使钡离子转化为沉淀,硫化氢只能使铜离子转化为沉淀,过量NaOH只能使镁离子转化为沉淀,滤液中通入足量二氧化碳可使偏铝酸根离子转化为沉淀,则使Ag+、Cu2+、Mg2+、Ba2+、Al3+等离子,逐一沉淀分离,所加试剂及顺序为NaCl→Na2SO4→H2S→NaOH→CO2,
故选D.
点评 本题考查离子的检验及分离,为高频考点,把握离子的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意离子逐一沉淀的限制条件,题目难度不大.


 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源:2016-2017学年甘肃省高二上第一次学段考试化学卷(解析版) 题型:选择题
已知一定条件下断裂1 mol下列化学键生成气态原子需要吸收的能量如下:H—H 436 kJ;Cl—Cl 243 kJ;H—Cl 431 kJ。下列所得热化学方程式或结论正确的是( )
A.H(g)+Cl(g)=HCl(g)ΔH=﹣431kJ·mol-1
B.2HCl(g)=H2(g)+Cl2(g)的反应热ΔH<0
C.H 2(g)+Cl2(g)=2HCl(g)ΔH=﹣183kJ
2(g)+Cl2(g)=2HCl(g)ΔH=﹣183kJ
D.相同条件下,H2(g)+Cl2(g)=2HCl(g)反应在光照和点燃条件下的ΔH不相等
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
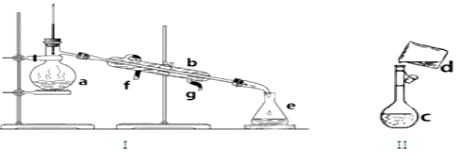
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是放热反应都是自发的,凡是吸热反应都是非自发的 | |
| B. | 自发反应一定是放热反应,非自发反应一定是吸热反应 | |
| C. | 自发反应在恰当条件下才能实现 | |
| D. | 自发反应在任何条件下都能实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
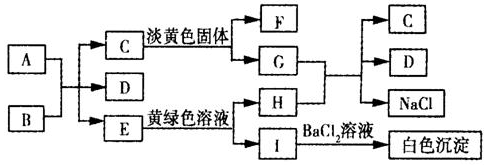
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
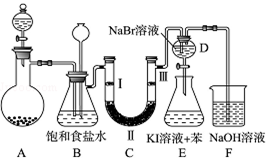
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com