
江苏宝胜集团是一家以生产电缆产品为主的大型企业.在电缆的生产过程中,不可避免地产生一定量的含铜废料
(如零碎电缆).某化学兴趣小组的四位同学得知这一情况后,围绕“从含铜废料中回收铜”提出了各自的看法.甲同学根据已学知识,提出了一套回收方案:
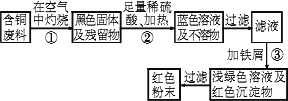
乙同学在查阅资料后得知:在通入空气并加热的条件下,铜可以与稀硫酸在溶液中发生反应
(反应的化学方程式为2Cu+2H2SO4+O2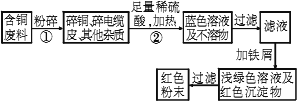
(1)从环保角度对两套方案的不同部分进行比较,
你认为________(填“甲”或“乙”)方案更合理.理由是________________.
(2)丙认为,无论是甲方案还是乙方案,在“加铁屑”这一步时,应加入略过量的铁屑,理由是________________.为此丁又提出了疑问:如果铁过量,剩余的铁会混在红色粉末中,该怎么处理呢?请你给出合理的建议:________.
(3)最后,老师肯定了同学们的思考,同时指出:方案中最后一步所得的浅绿色滤液结晶后,会得到一种俗称“绿矾”的工业产品,可以增加经济效益.请写出两种可以使“绿矾”结晶的方法:________、________(“绿矾”的溶解度随温度的升高而增大).如果直接排放滤液,不仅造成浪费,还会________.
答案:
(1)乙 甲方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾(关键词:污染空气)(2)确保CuSO4完全反应(或将Cu完全置换出来,其他类似的说法均可) 将所得的铜粉酸洗后再洗涤、干燥(或过滤前在加入适量的酸以除去剩余的铁粉)
(3)蒸发 降温 造成水污染(或环境污染)
讲析:本题是对两种回收铜的方案进行对比探究的开放型试题.甲方案比乙方案多一步灼烧,由此带入污染.除杂或是制取物质时,加入的反应物有一种应过量,目的是确保另一物质全部反应.铁、铜的分离可以依据两者的活动性差异采取酸溶法.
FeSO4溶液通过蒸发水分或是降低温度,均可以析出晶体.滤液中含有Fe2+,是重金属盐,对水体有污染.点评:此题为贯穿环保知识的试题,设置的问题大多并无确切的答案,答题时只要注意到关键字即可.


科目:高中化学 来源:启东市汇龙中学迎二模模拟考试(二)、化学 题型:058
| |||||||||||||||||||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com