
| A�� | ԭ�Ӱ뾶��W��Z��Y��X��M | |
| B�� | XZ2��X2M2��W2Z2��Ϊֱ���͵Ĺ��ۻ����� | |
| C�� | ��XԪ���γɵĵ��ʿ��ܵ��� | |
| D�� | ��X��Y��Z��M����Ԫ���γɵĻ�����һ���������Ӽ������й��ۼ� |
���� X��Y��Z��M��WΪ���ֶ�����Ԫ�أ�X��Y��Z��ԭ���������ε�����ͬ����Ԫ�أ�������������֮��Ϊ15��������������ƽ��Ϊ5��X��Z���γ�XZ2��̬���ӣ�XΪ+4�ۣ�YΪ-2�ۣ���֪X��Y��Z�ֱ�ΪC��N��O����Ԫ�أ�Y��M�γɵ���̬�������ڱ�״���µ��ܶ�0.76g•L-1�������̬�������Ħ������Ϊ22.4L/mol��0.76g•L-1=17g/mol���Ӷ�ȷ��MΪHԪ�أ�W����������X��Y��Z��M����Ԫ��������֮�͵�$\frac{1}{2}$���Ƴ�W��������Ϊ$\frac{1}{2}$����6+7+8+1��=11����WΪNaԪ�أ��Դ������
��� �⣺������������֪��XΪC��YΪN��ZΪO��MΪH��WΪNa��
A�����Ӳ�Խ�࣬ԭ�Ӱ뾶Խ��ͬ���ڴ�������ԭ�Ӱ뾶��С����ԭ�Ӱ뾶��W��X��Y��Z��M����A����
B��X2M2Ϊֱ���͵Ĺ��ۻ����W2Z2Ϊ���ӻ����XZ2Ϊ���ۻ��������ֱ���ͣ�����B����
C����XԪ���γɵĵ���Ϊʯīʱ���ɵ��磬��C��ȷ��
D����X��Y��Z��M����Ԫ���γɵĻ��������Ϊ���ۻ�����������Ӽ����簱���ᣬ��D����
��ѡC��
���� ���⿼��ԭ�ӽṹ��Ԫ�������ɣ�Ϊ��Ƶ���㣬����ԭ�ӽṹ����������ϵ��Ħ�������ƶ�Ԫ��Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��Ԫ�ػ�����֪ʶ��Ӧ�ã���Ŀ�ѶȲ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��2 | B�� | 8��1 | C�� | 1��1 | D�� | 800��108 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ���ʱ�Ϊ��ֵ | |
| B�� | �����¶ȣ�����Ӧ���������淴Ӧ���ʼ�С��ƽ�������ƶ� | |
| C�� | 2CO2��g��+2H2��g��?2CO��g��+2H2O��g�� ��ƽ�ⳣ��K1=K2 | |
| D�� | �����ݡ������³���CO����Kֵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ĺ��������ǻ� | |
| B�� | �ǻ����������к��еĵ�������ͬ | |
| C�� | ��������ȼ��ֻ���ɶ�����̼��ˮ���л���һ������ | |
| D�� | �Ҵ����Ʒ�Ӧ����������������˵���Ҵ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ǧ���صķŵ練Ӧ | B�� | �����������ڸ����µķ�Ӧ | ||
| C�� | ������ˮ�ⷴӦ | D�� | ̿��CO2�Ļ��Ϸ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
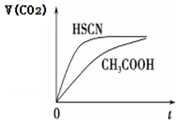 ��֪25��ʱ����������ʵĵ���ƽ�ⳣ�����������
��֪25��ʱ����������ʵĵ���ƽ�ⳣ�����������| ���ữѧʽ | HSCN | CH3COOH | HCN | H2CO3 |
| ����ƽ�ⳣ�� | 1.3��10-1 | 1.7��10-5 | 6.2��10-10 | K1=4.3��10-7 K2=5.6��10-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ���ܱ������з�����Ӧ��X+2Y?2Z����H��0��������Z����̬����Z��ƽ�������е����������Z%�����¶ȣ�T����ѹǿ��P���Ĺ�ϵ��ͼ�������ж���ȷ���ǣ�������
���ܱ������з�����Ӧ��X+2Y?2Z����H��0��������Z����̬����Z��ƽ�������е����������Z%�����¶ȣ�T����ѹǿ��P���Ĺ�ϵ��ͼ�������ж���ȷ���ǣ�������| A�� | Yһ������̬ | |
| B�� | T1����T2 | |
| C�� | �����¶ȣ��÷�Ӧ�Ļ�ѧƽ�ⳣ������ | |
| D�� | ��c��X����c��Y����c��Z��=1��2��2ʱ����Ӧ�ﵽƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 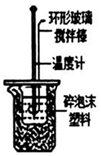 ��ͼ��ʾװ�òⶨ�кͷ�Ӧ�ķ�Ӧ�� | |
| B�� |  ��ͼ��ʾװ����ʵ������ȡ������ϩ | |
| C�� | 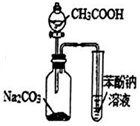 ��ͼ3��ʾװ��֤��̼������ǿ�ڱ��� | |
| D�� | 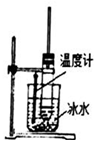 ��ͼ��ʾװ����ʵ������ȡ���������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com