
【题目】按要求完成下列填空:
(1)写 出“海洋元素”的元素符号_______ ,该元素单质的苯溶液颜色为_______。
(2)写出NaCl的电子式________ 。
(3)NaHCO3溶于水的电离方程式_________。
(4)写出实验室用MnO2与 浓HCl制氯气的离子方程式__________。
(5)用化学方程式表示除去Na2CO3固体中混有的NaHCO3__________。
(6)完成下列氧化还原反应的离子方程式( )MnO4-+( )SO2+ _____=( )Mn2++( )SO42-+______。____________
【答案】 Br 橙红色 ![]() NaHCO3=Na++HCO3- MnO2+2Cl-+4H+
NaHCO3=Na++HCO3- MnO2+2Cl-+4H+![]() Mn2++Cl2↑+2H2O 2NaHCO3
Mn2++Cl2↑+2H2O 2NaHCO3![]() Na2CO3+H2O+CO2↑ (2)MnO4-+(5)SO2+ 2H2O=(2)Mn2++(5)SO42ˉ+ 4H+
Na2CO3+H2O+CO2↑ (2)MnO4-+(5)SO2+ 2H2O=(2)Mn2++(5)SO42ˉ+ 4H+
【解析】(1)溴元素有百分之九十九存在于海洋中,人们叫它为“海洋元素”;溴易溶于苯中得到溴的苯溶液,呈现出橙红色。
(2)NaCl为离子化合物,成键粒子为阴阳离子,电子式为:![]() 。
。
(3)NaHCO3溶于水电离出Na+和HCO3-,电离方程式为:NaHCO3=Na++HCO3-。
(4)MnO2与 浓HCl制氯气的离子方程式为:MnO2+2Cl-+4H+![]() Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。
(5)Na2CO3固体中混有的NaHCO3,可以利用NaHCO3的不稳定性,加热将其分解除去,化学方程式为:2NaHCO3![]() Na2CO3+H2O+CO2↑ 。
Na2CO3+H2O+CO2↑ 。
(6)一般,缺项配平中,缺项的物质没有参与氧化还原反应,因此可以根据得失电子守恒先配平氧化剂、还原剂、氧化产物和还原产物前的系数, MnO4-、SO2、Mn2+、SO42ˉ前的系数分别为2、5、2、5,根据电荷守恒可知,右边负电多于左边,所以右边补产物H+,左边加H2O,再根据电荷守恒和质量守恒配平,最后完整的离子方程式为:2 MnO4-+5SO2+ 2H2O=2n2++5SO42ˉ+ 4H+。


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. MgCO3![]() MgCl2(aq)
MgCl2(aq)![]() Mg
Mg
B. NaCl(aq)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
C. Cu2(OH)2CO3![]() CuO
CuO![]() Cu(OH)2
Cu(OH)2
D. SO2![]() NH4HSO3
NH4HSO3![]() (NH4)2SO4
(NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于电解质溶液的正确判断是( )
A.在pH=12的溶液中,K+、Cl﹣、HCO3﹣、Na+可以共存
B.水电离的c(H+)=1×10﹣3mol/L的溶液中:Na+、Fe3+、SO42﹣、Cl﹣
C.由0.l moI/L BOH溶液的pH=10,可推知BOH溶液存在BOH=B++OH﹣
D.![]() =1×10﹣13mol/L 的溶液中:Ba2+、ClO﹣、Cl﹣、NO3﹣
=1×10﹣13mol/L 的溶液中:Ba2+、ClO﹣、Cl﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.10molL﹣1的标准NaOH溶液滴定未知浓度的盐酸,取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂.重复上述滴定操作2~3 次,记录数据如下.
(1)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有 .
A.滴定前平视读数,终点读数时仰视读数
B.锥形瓶水洗后未用用标准盐酸润洗
C.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗
D.标准液漏滴在锥形瓶外一滴
E.滴定前仰视读数,终点滴定后俯视读数
F.碱式滴定管尖嘴部分有气泡,滴定后消失
(2)若在达到滴定终点时,不慎多加了一滴NaOH溶液(一滴溶液体积约为0.05mL)继续加水到50mL,所得溶液的PH为
(3)如图是向20mL的盐酸中逐渐加入0.1mol/L NaOH溶液时,溶液的pH变化图象,当滴加NaOH溶液为10mL时,该混合液的PH= , (含Lg表达式),若用该NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述中正确的是
A.溶液呈中性,可选用甲基橙或酚酞作指示剂 B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂 D.溶液呈碱性,只能选用酚酞作指示剂
(4)氧化还原滴定﹣﹣取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1molL﹣1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O.表格中记录了实验数据:
数 | 待测液体积 | 标准KMnO4溶液体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 25.00 | 0.50 | 23.40 |
第二次 | 25.00 | 4.00 | 23.90 |
第三次 | 25.00 | 5.00 | 25.10 |
①滴定时,滴定终点时滴定现象是
②该草酸溶液的物质的量浓度为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验过程中对应的变化与右图相符合的是
实验过程 | X | Y |
| |
A | 稀HCl滴加到NaOH溶液中 | V(HCl) | N(Na+) | |
B | 铁粉加入 CuSO4溶液中 | m(Fe) | m(固 体) | |
C | CO2通入NaOH溶液中 | V(CO2) | 溶液的导电能力 | |
D | 稀H2SO4滴加到 Ba(OH)2溶液中 | V(H2SO4) | 溶液的导电能力 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿斯巴甜是目前使用最广泛的甜味剂.甜度约为蔗糖的200倍,其结构简式为: 
下列关于阿斯巴甜的说法正确的是( )
A.分子式为C14H19N2O5
B.既能与酸反应又能与碱反应
C.不能发生水解反应
D.1mol该物质最多可与2molNaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业用氧化铝与焦炭在氮气流中加强热制备氮化铝(AlN),氮化铝样品中含少量Al4C3、C、Al2O3杂质。某实验小组拟测定ag氮化铝样品中Al4C3含量并探究甲烷与氧化铜反应的氧化产物为CO2。
已知:(Ⅰ)AlN、Al4C3都能与水反应,分别生成NH3、CH4。
(Ⅱ)CH4还原氧化铜:CH4+4CuO![]() 4Cu+CO2+2H2O。
4Cu+CO2+2H2O。
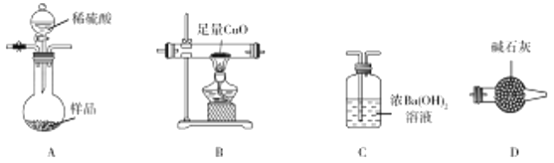
(1)装置连接顺序为 ________________________(按气流从左至右)。
(2)写出A中发生反应的化学方程式:AlN和稀硫酸反应:__________________________;Al4C3与
稀硫酸反应:_______________________________________________________________________。
(3)有下列操作步骤:
①缓缓向A中通入一定量的N2。
②称量B(酒精灯、木块和铁架台除外),按顺序组装仪器,检查装置的气密性,将样品放入烧瓶中;
③点燃B处酒精灯;
④再次称量B;
⑤从分液漏斗中缓慢滴入稀硫酸,直到不再产生气体为止;
⑥再次缓慢通入一定量的N2。
正确的操作顺序是_________________________;操作①的目的是_______________;若操作③与操作⑤顺序颠倒, 将导致测得的Al4C3的质量分数_________(填“偏大”“偏小”或“不变”)。
(4)设计实验证明A中有NH4+生成:__________________________________。
(5)实验结束后,测得B中固体质量减少bg,则样品中Al4C3的质量分数为________×100%。
(6)通过测定C中生成BaCO3的质量可以确定甲烷与氧化铜反应是否有CO生成。实验完毕后,测得B
中固体质量减少bg;对C中混合物进行过滤、洗涤、干燥、称重,当m(BaCO3)=________g时(用含b表达式表示),表明氧化产物只有CO2。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com