
| A�� | �ö��Ե缫���NaH2PO2��Һ����������ӦʽΪ��2H2O-4e-�TO2��+4H+ | |
| B�� | H3PO2�����NaOH��Һ��Ӧ�����ӷ���ʽΪ��H3PO2+3OH-�TPO23-+3H2O | |
| C�� | ��H3PO2��Һ���뵽�����ظ������Һ�У�H3PO2�Ļ�ԭ�������ΪH3PO4 | |
| D�� | H3PO2����ˮ�ĵ��뷽��ʽΪH3PO2?H++H2PO2- |
���� A��H3PO2���н�ǿ�Ļ�ԭ�ԣ����ʱ��������H2PO2-ʧ���ӣ�
B��һԪ������NaOH�������ʵ���1��1��Ӧ��
C��H3PO2���л�ԭ�ԣ��ܱ��������������
D��һԪ��������Һ�в��ֵ����һ�������ӣ�
��� �⣺A��H3PO2���н�ǿ�Ļ�ԭ�ԣ����ʱ��������H2PO2-ʧ���ӣ������ö��Ե缫���NaH2PO2��Һ����������ӦʽΪH2PO2--4e-+2H2O�TH3PO4+3H+����A����
B��һԪ������NaOH�������ʵ���1��1��Ӧ������H3PO2�����NaOH��Һ��Ӧ�����ӷ���ʽΪ��H3PO2+OH-�TH2PO2-+H2O����B����
C��H3PO2���л�ԭ�ԣ��ܱ����������������H3PO2��Һ���뵽���Ը��������Һ�У�H3PO2����������ΪH3PO4����C����
D��һԪ��������Һ�в��ֵ����һ�������ӣ���H3PO2����ˮ�ĵ��뷽��ʽΪ��H3PO2?H++H2PO2-����D��ȷ��
��ѡD��
���� ���⿼��������ԭ��Ӧ�����뷽��ʽ����д�����ԭ����Ӧ�õ�֪ʶ�㣬��ȷ���ʵ������ǽⱾ��ؼ������õ缫����ʽ����д���������뷽��ʽ��д��������ˮ��ԭ����ɣ���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
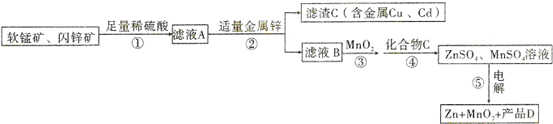
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ҺNaOH��Һȡ����ƿ��¶�ÿ����нϳ�ʱ�䣬�Է�̪Ϊָʾ���ⶨ | |
| B�� | �Լ���Ϊָʾ���������ȱ��ʱֹͣ�ζ� | |
| C�� | ��Һ��������ˮ��ϴ��ֱ����ȡ����Һ | |
| D�� | �ζ��յ����ʱ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
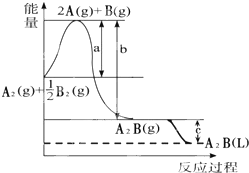 ��֪��A2��g��+$\frac{1}{2}$B2��g���TA2B��g������Ӧ�����������仯��ͼ���ʣ�
��֪��A2��g��+$\frac{1}{2}$B2��g���TA2B��g������Ӧ�����������仯��ͼ���ʣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8.67---9.26 | B�� | 7.00 | C�� | 7.35---7.45 | D�� | ����5.70 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
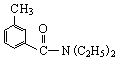 �� DEET��һ�������£���ͨ�������·�����ϳɣ�
�� DEET��һ�������£���ͨ�������·�����ϳɣ�
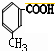 ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ӳ�ȴ� | |
| B�� | �ۡ��е�ϵ� | |
| C�� | ���� | |
| D�� | ���н��������硢���ȡ�����չ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com