
分析 向合金与盐酸反应所得溶液中滴入硫氰化钾溶液不变色,说明生成FeCl2,同时生成氢气,发生反应:Fe+Fe2O3+6HCl=3FeCl2+3H2O,Fe+2HCl=FeCl2+H2↑,根据氢气计算与HCl反应Fe的物质的量,反应后溶液中再通入氯气,FeCl2被氧化为FeCl3,根据电子转移守恒计算n(FeCl2),再根据Fe原子守恒计算合金未被氧化时铁的物质的量,结合Fe+Fe2O3+6HCl=3FeCl2+3H2O计算Fe2O3的物质的量,未被氧化时合金的质量=19.4g-氧化铁中氧元素质量,进而计算合金未被氧化时铁的质量分数.
解答 解:向合金与盐酸反应所得溶液中滴入硫氰化钾溶液不变色,说明生成FeCl2,同时生成氢气,发生反应:Fe+Fe2O3+6HCl=3FeCl2+3H2O,Fe+2HCl=FeCl2+H2↑,
生成氢气为$\frac{3.36L}{22.4L/mol}$=0.15mol,则与盐酸反应Fe的物质的量为0.15mol,
再通入氯气,FeCl2被氧化为FeCl3,消耗氯气物质的量为$\frac{3.36L}{22.4L/mol}$=0.15mol,根据电子转移守恒,n(FeCl2)=$\frac{0.15mol×2}{3-2}$=0.3mol,根据Fe原子守恒n(Fe)=n(FeCl2)=0.3mol,由Fe+Fe2O3+6HCl=3FeCl2+3H2O,可知Fe2O3的物质的量为(0.3mol-0.15mol)×$\frac{2}{3}$×$\frac{1}{2}$=0.05mol,
则未被氧化时合金的质量=19.4g-0.05mol×3×16g/mol=17g,
合金未被氧化时铁的质量为0.3mol×56g/mol=16.8g,则合金未被氧化时铁的质量分数=$\frac{16.8g}{19.4g}$×100%=98.8%,
答:合金未被氧化时铁的质量分数为98.8%.
点评 本题考查混合物计算,侧重对学生分析计算能力与解题方法技巧的考查,注意利用守恒法与总反应方程式计算计算解答.


 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 上海世博会很多场馆的外墙使用的非晶体薄膜,以充分利用天阳能,体现低碳经济 | |
| B. | 金属的电化学防护措施有牺牲阳极的阴极保护法和外加电流的阴极保护法 | |
| C. | 若在水果贮藏室中,放几块被KMnO4溶液浸透过的“砖块”,可延长水果保存时间 | |
| D. | 常温时,某可逆反应的平衡常数越大则其反应速率就越快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖可通过酒化酶水解生成酒精 | |
| B. | 分子式为CH4O和C2H6O的物质一定互为同系物 | |
| C. | 向植物油中加入酸性高锰酸钾紫色溶液,振荡后,酸性高锰酸钾溶液颜色褪去 | |
| D. | 淀粉溶液与稀硫酸溶液共热,再加入新制氢氧化铜悬浊液加热,无红色沉淀,则可证明淀粉没有水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
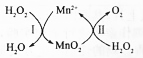 MnSO4可用作催化剂和生产微量元素肥料等,回答下列问题:
MnSO4可用作催化剂和生产微量元素肥料等,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 起始温度T1/℃ | 终止温度T2/℃ | 温度差(T2-T1)/℃ | |||
| HCl | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.5 | 24.50 | 27.5 | 3.00 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
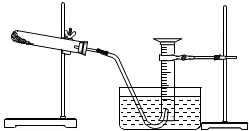 某同学完成以胆矾为原料制取氧化铜固体实验,并用氧化铜和氯酸钾的混合物制取氧气,测量生成氧气的体积.试回答:
某同学完成以胆矾为原料制取氧化铜固体实验,并用氧化铜和氯酸钾的混合物制取氧气,测量生成氧气的体积.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
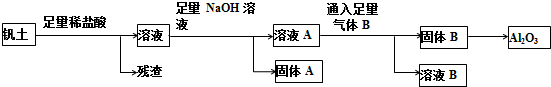
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com