
 CӢ
C”¢ ·Ö±š°“ĻĀŹ½·“Ó¦£ØČ¼ÉÕ£©£ŗ
·Ö±š°“ĻĀŹ½·“Ó¦£ØČ¼ÉÕ£©£ŗ ·ÅČČ
·ÅČČ
 ·ÅČČ
·ÅČČ
 ·ÅČČ
·ÅČČ

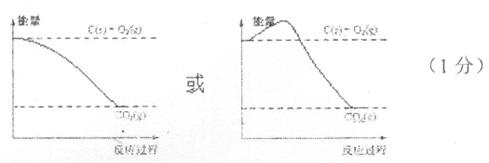


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ä¾ĢæŌŚæÕĘųÖŠČ¼ÉÕ |
| B£®ĒāĘųŌŚĀČĘųÖŠČ¼ÉÕ |
| C£®ŃĪĖįŗĶĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦ |
| D£®½«Ba(OH)2”¤8H2O¾§ĢåŗĶNH4C1¾§ĢåŃŠĻøŗó»ģŗĻ²¢½Į°č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
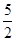 O2(g) ="=" 2CO2(g)£«H2O(l) ¦¤H1£½-1301.0 kJ?mol-1
O2(g) ="=" 2CO2(g)£«H2O(l) ¦¤H1£½-1301.0 kJ?mol-1| A£®+228.2 kJ”¤mol-1 | B£®-228.2 kJ”¤mol-1 |
| C£®+1301.0 kJ”¤mol-1 | D£®+621.7 kJ”¤mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĪļÖŹ·¢Éś»Æѧ·“Ó¦¶¼°éĖę×ÅÄÜĮæ±ä»Æ |
| B£®°éÓŠÄÜĮæ±ä»ÆµÄĪļÖŹ±ä»Æ¶¼ŹĒ»Æѧ±ä»Æ |
| C£®ŌŚŅ»øöČ·¶ØµÄ»Æѧ·“Ó¦¹ŲĻµÖŠ£¬·“Ó¦ĪļµÄ×ÜÄÜĮæÓėÉś³ÉĪļµÄ×ÜÄÜĮæŅ»¶Ø²»Ķ¬ |
| D£®ŌŚŅ»øöČ·¶ØµÄ»Æѧ·“Ó¦¹ŲĻµÖŠ£¬·“Ó¦ĪļµÄ×ÜÄÜĮæ²»Ņ»¶Ø×ÜŹĒøßÓŚÉś³ÉĪļµÄ×ÜÄÜĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®°×Į×ŌŚøō¾ųæÕĘųµÄĢõ¼žĻĀ£¬ŌŚ260”ę×Ŗ»ÆĪŖŗģĮ× |
| B£®ŹÆÄ«ŌŚøßĪĀøßŃ¹ĻĀ×Ŗ»ÆĪŖ½šøÕŹÆ |
| C£®øɱł×Ŗ»ÆĪŖCO2ĘųĢå |
| D£®¹ĢĢ¬S8¼ÓČȵ½444.6”ꏱ±ä³ÉĮņÕōĘųS2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©| A£®ĖłÓŠ»Æѧ±ä»ÆŅ»¶Ø×ńŃÖŹĮæŹŲŗćŗĶÄÜĮæŹŲŗć |
| B£®ĖłÓŠ»Æѧ±ä»ÆµÄÄÜĮ涼æÉŅŌĶعżŌµē³Ų×Ŗ»ÆĪŖµēÄÜ |
| C£®»Æѧ¼üµÄ±ä»Æ±ŲČ»»įŅżĘšÄÜĮæ±ä»Æ£¬ĖłŅŌ£¬ÄÜĮæ±ä»ÆŅ²Ņ»¶Ø»įŅżĘš»Æѧ±ä»Æ |
| D£®¶ĻæŖ¾É»Æѧ¼üÓėŠĪ³ÉŠĀ»Æѧ¼üÖ®¼äµÄÄÜĮæ²īÖ»ÄÜŅŌČČĮæµÄŠĪŹ½ŹĶ·Å |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com