
 在“天宫二号”上蚕宝宝的“太空屋”形似胶囊(如图),两端的半球体由航天铝合金打造,中间部分采用透明有机玻璃,蚕宝宝由聚氨酯海绵包裹着.
在“天宫二号”上蚕宝宝的“太空屋”形似胶囊(如图),两端的半球体由航天铝合金打造,中间部分采用透明有机玻璃,蚕宝宝由聚氨酯海绵包裹着. 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:实验题
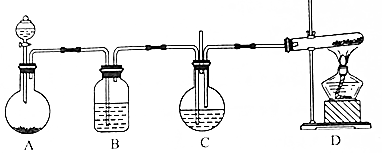
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若X、Y同主族,则X、Y的单质间不能发生反应 | |
| B. | 若X、Y同周期,则X、Y之间只能形成离子化合物 | |
| C. | 若X为磷元素,则Y与X之间可形成两种化合物 | |
| D. | 若X为铝元素,则Y的最高价氧化物对应的水化物为强酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9.0g草酸中共用电子对数目为0.9NA | |
| B. | 9.0g草酸被NaClO氧化生成CO2,转移的电子数为0.2NA | |
| C. | 9.0g草酸溶于水,其中C2O${\;}_{4}^{2-}$和HC2O${\;}_{4}^{-}$的微粒数之和为0.1NA | |
| D. | 9.0g草酸受热完全分解为CO2、CO、H2O,标准状况下测得生成的气体体积为4.48L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
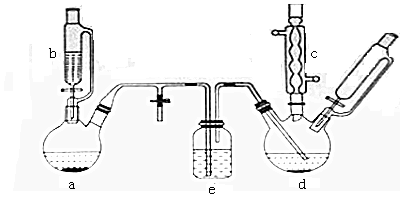
| 有机物 | 苯 | 氯苯 | 邻二氯苯 | 间二氯苯 | 对二氯苯 |
| 沸点/℃ | 80 | 132.2 | 180.4 | 173.0 | 174.1 |
| 流失项目 | 蒸气挥发 | 二氯苯 | 其他 | 合计 |
| 苯流失量(kg/I) | 28.8 | 14.5 | 56.7 | 100 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
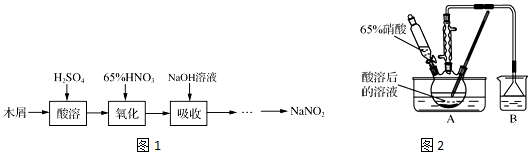
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
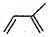 )是合成天然橡胶的单体.请回答下列问题:
)是合成天然橡胶的单体.请回答下列问题: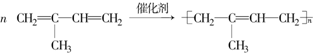 ,该反应类型为加聚反应.
,该反应类型为加聚反应.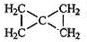 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com