
【题目】功能高分子P的合成路线如下:

(1)A的分子式是C7H8,其结构简式是__________________________。
(2)试剂a是_____________________。
(3)反应③的化学方程式:__________________________________________。
(4)E的分子式是C6H10O2。E中含有的官能团:_____________________。
(5)反应④的反应类型是_____________________________。
(6)反应⑤的化学方程式:________________________________________。
(7)已知: 。以乙烯为起始原料,选用必要的无机试剂合成E,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________________。
。以乙烯为起始原料,选用必要的无机试剂合成E,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)___________________。
【答案】![]() 浓HNO3和浓H2SO4
浓HNO3和浓H2SO4 ![]() +NaOH
+NaOH![]()
![]() +NaCl 碳碳双键、酯基 加聚反应
+NaCl 碳碳双键、酯基 加聚反应 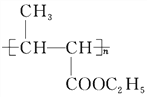 +nH2O
+nH2O![]()
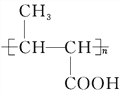 +nC2H5OH H2C===CH2
+nC2H5OH H2C===CH2![]() C2H5OH
C2H5OH![]() CH3CHO
CH3CHO![]()
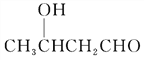
![]() CH3CH===CHCHO
CH3CH===CHCHO![]() CH3CH===CHCOOH
CH3CH===CHCOOH![]() CH3CH===CHCOOC2H5
CH3CH===CHCOOC2H5
【解析】
A的分子式是C7H8,其结构简式是![]() ,结合P的结构简式,可知A与浓硝酸在浓硫酸、加热条件下发生取代反应生成B为
,结合P的结构简式,可知A与浓硝酸在浓硫酸、加热条件下发生取代反应生成B为![]() ,B与氯气在光照条件下发生取代反应生成C为
,B与氯气在光照条件下发生取代反应生成C为![]() ,C在氢氧化钠水溶液、加热条件下发生水解反应生成D为
,C在氢氧化钠水溶液、加热条件下发生水解反应生成D为![]() ,可知G的结构简式
,可知G的结构简式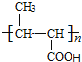 ,则F,E的分子式是C6H10O2,则E为CH3CH=CHCOOCH2CH3;
,则F,E的分子式是C6H10O2,则E为CH3CH=CHCOOCH2CH3;
(1)A的分子式是C7H8,其结构简式是![]() ;
;
(2)试剂a是:浓硫酸和浓硝酸,故答案为:浓硫酸和浓硝酸;
(3)反应③的化学方程式:![]() +NaOH
+NaOH![]()
![]() +NaCl;
+NaCl;
(4)E为CH3CH=CHCOOCH2CH3,E中含有的官能团:碳碳双键、酯基;
(5)反应④的反应类型是:加聚反应;
(6)反应⑤的化学方程式 +nH2O
+nH2O![]()
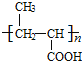 +n CH3CH2OH;
+n CH3CH2OH;
(7)乙烯与HBr发生加成反应生成CH3CH2Br,然后发生水解反应生成CH3CH2OH,再发生氧化反应生成CH3CHO,2分子乙醛发生加成反应生成![]() ,再发生氧化反应生成
,再发生氧化反应生成![]() ,再与氢气发生加成反应生成
,再与氢气发生加成反应生成![]() ,在浓硫酸、加热条件下发生消去反应生成生成CH3CH=CHCOOH,最后与乙醇发生酯化反应生成CH3CH=CHCOOCH2CH3,合成路线流程图为:H2C=CH2
,在浓硫酸、加热条件下发生消去反应生成生成CH3CH=CHCOOH,最后与乙醇发生酯化反应生成CH3CH=CHCOOCH2CH3,合成路线流程图为:H2C=CH2![]() C2H5OH
C2H5OH![]() CH3CHO
CH3CHO![]()
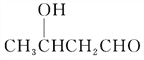
![]() CH3CH=CHCHO
CH3CH=CHCHO![]() CH3CH=CHCOOH
CH3CH=CHCOOH![]() CH3CH=CHCOOC2H5。
CH3CH=CHCOOC2H5。


科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.1mol H2O的质量为18g/mol
B.CH4的摩尔质量为16g
C.3.01×1023个Cl2分子的质量为35.5g
D.标准状况下,1mol任何物质的体积均约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法不正确的是( )
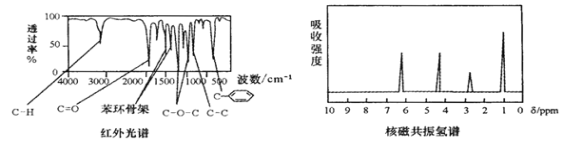
A. 由红外光谱可知,A中含有C-H键、C=O键、![]() 等
等
B. 由核磁共振氢谱可知,该有机物分子中有4种不同化学环境的氢原子
C. 若A的化学式为C8H8O2,则其结构简式可能为![]()
D. 由以上信息可以推测A分子可能为含有酯基的芳香族化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,体积为2L的密闭容器中,NO2和N2O4之间发生反应:2NO2(g)(红棕色)![]() N2O4g)(无色),如图所示.
N2O4g)(无色),如图所示.
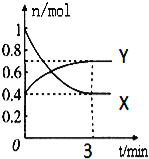
(1)曲线 (填“X”或“Y”)表示NO2的物质的量随时间的变化曲线.
(2)若降低温度,则v(正) ,v(逆) .(填“加快”或“减慢”或“不变”).
(3)若上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(NO2)=0.3mol/(Ls),乙中v(N2O4)=6mol/(Lmin),则 中反应更快.
(4)在0到3min中内N2O4的反应速率为 .
(5)下列叙述能说明该反应已达到化学平衡状态的是(填标号) ;
A.v(NO2)=2v(N2O4) |
B.容器内压强不再发生变化 |
C.X的体积分数不再发生变化 |
D.容器内气体原子总数不再发生变化 |
E.相同时间内消耗n mol的Y的同时生成2n mol的X
F.相同时间内消耗n mol的Y的同时消耗2n mol的X.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下刎有关实验装置、操作,不能实现相应实验目的的是

A. 装置甲可用酸性KMnO4溶液滴定FeSO4溶液
B. 用装置乙进行实验时若逐滴滴加AgNO3溶液先出现黄色沉淀,可说明 Ksp(AgCl)>Ksp(AgI)
C. 装置丙可用于收集氢气
D. 装置丁可用于 NaOH溶液除去溴苯中单质溴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固定容积为2L的密闭容器中发生反应xA(g)+yB(g)![]() zC(g),图I表示t℃时容器中各物质的量随时间的变化关系,图II表示平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是
zC(g),图I表示t℃时容器中各物质的量随时间的变化关系,图II表示平衡常数K随温度变化的关系。结合图像判断,下列结论正确的是
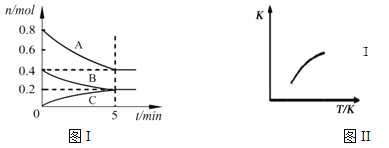
A. 该反应可表示为:2A(g)+B(g)![]() C(g)ΔH﹤0
C(g)ΔH﹤0
B. t℃时该反应的平衡常数K=6.25
C. 当容器中气体密度不再变化时,该反应达到平衡状态
D. t℃,在第6 min时再向体系中充入0.4 mol C,再次达到平衡时C的体积分数大于0.25
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)实验过程中铜网出现黑色和红色交替的现象,请写出相应的化学方程式______________________________、________________________________。
(2)甲水浴的作用是_________________________________________;乙水浴的作用是_________________________________________。
(3)反应进行一段时间后,干试管a中能收集到不同的物质,它们是________。集气瓶中收集到的气体的主要成分是________。
(4)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有______。要除去该物质,可在混合液中加入____________(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】F可用作丙烯酸酯橡胶的基材。以煤为原料制取F的一种合成路线如下:

(1)①的加工手段称为煤的_______(填“气化”“液化”或“干馏”)。
(2)②、④反应类型依次是______、______。
(3)E中所含官能团名称是_______和_______。
(4)C与A互为同系物,C的化学名称是_______;F的结构简式为_______。
(5)反应④的化学方程式为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com