
| A. | CO和HCl | B. | H2,HCl和CO | C. | CO2,CO和HCl | D. | CO2,CO |
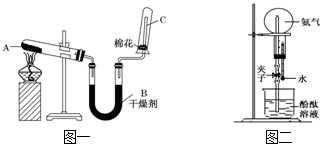
分析 某气体可能含有NH3、HCl、CO、H2、CO2中的一种或几种,在恒温恒压下将其通过浓硫酸时,总体积基本不变,可知混合气体中不含NH3;根据通过过量的澄清石灰水,未见变浑浊,但混合气体的总体积减小,说明有气体被吸收;在O2中能够点燃,燃烧产物不能使CuSO4粉末变色说明没有水蒸气生成进行解答.
解答 解:某气体可能含有NH3、HCl、CO、H2、CO2中的一种或几种,在恒温恒压下将其通过浓硫酸时,总体积基本不变,可知混合气体中不含NH3;通过过量的澄清石灰水,未见变浑浊,一定不含二氧化碳气体,但混合气体的总体积减小,说明有气体被吸收,只能是HCl气体,说明含有HCl;在O2中能够点燃,燃烧产物不能使CuSO4粉末变色说明没有氢气,故原混合气体中含有HCl和CO,没有氢气和二氧化碳气体,故选A.
点评 本题考查混合气体的组成判断,难度不大,做题时注意从物质反应的典型现象入手判断.


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
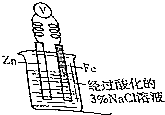 钢铁是用量最大、用途最广的合金,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命.
钢铁是用量最大、用途最广的合金,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 加入试剂 | 被检出物质 | 理由 |
| 水 | CuSO4 | CuSO4溶于水溶液显蓝色 |
| 加入试剂 | 被检出物质 | 离子方程式 |
| CuSO4 |
| 加入试剂 | 被检出物质 | 离子方程式 |
| MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2g氢气所含原子数目为NA | |
| B. | 标准状况下,11.2L H2O所含分子数为0.5NA | |
| C. | 1mol•L-1 CaCl2溶液中所含Ca2+离子的数目为NA | |
| D. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com