
分析 根据N2O4(g)?2NO2(g),△H>0,该反应为气体体积增大的吸热反应,根据平衡移动原理分析解答.
解答 解:(1)因为N2O4(g)?2NO2(g),△H>0,该反应为气体体积增大的吸热反应,所以保持容器体积不变,降低温度,平衡向放热方向即逆向移动,二氧化氮浓度减小,则混合气体的颜色变浅,故答案为:逆向;变浅;
(2)因为N2O4(g)?2NO2(g),△H>0,该反应为气体体积增大的吸热反应,所以保持温度不变,减小容器体积即增大压强,则反应速率加快,平衡向体体积减小即逆向移动,虽然二氧化氮物质的量减小,但减小容器体积,所以二氧化氮浓度仍然增大,所以混合气体的颜色变深,故答案为:加快;逆向;变深;
(3)保持容器体积和温度不变,通入N2,反应物生成物浓度不变平衡不移动,混合气体的颜色不变化,故答案为:不;不变化;
(4)保持容器压强和温度不变,通入Ar,体积增大,相当于减小反应体系的压强,则平衡向气体体积增大及正向移动,又体积增大,所以二氧化氮浓度减小,则混合气体的颜色变浅,故答案为:正向;变浅.
点评 本题主要考查了温度、压强对平衡移动的影响,难度不大,注意基础知识的积累.


科目:高中化学 来源: 题型:选择题
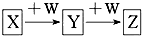 X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图所示转化关系(其他产物已略):下列说法不正确的是( )
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图所示转化关系(其他产物已略):下列说法不正确的是( )| A. | 若W是单质铁,则Z溶液可能是FeCl2溶液 | |
| B. | 若X是金属铝,则W可能是强碱 | |
| C. | 若W是氢氧化钠,则X与Z可能反应生成Y | |
| D. | 若X为氧气,则X与Y的相对分子质量可能相差12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
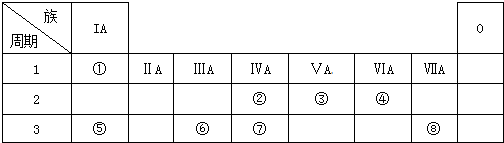
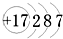
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 72.4% | B. | 71.4% | C. | 79.0% | D. | 63.6% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| b | |||||||||||||||||
| h | |||||||||||||||||
| a | f | i | j | l | m | ||||||||||||
| e | c | g | |||||||||||||||
| 锂 | X | |
| 第一电离能 | 519 | 580 |
| 第二电离能 | 7296 | 1820 |
| 第三电离能 | 11799 | 2750 |
| 第四电离能 | 11600 |
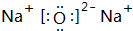 和
和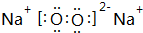 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
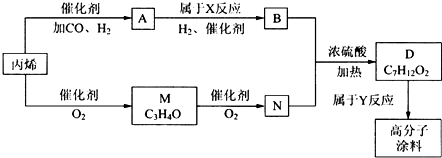
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10g甲烷中所含有的电子数目为10NA | |
| B. | 常温常压下,4g氦气所含有的质子数目为4NA | |
| C. | 标准状况下,22.4L单质溴所含有的原子数目为2NA | |
| D. | Fe-Cu和稀硫酸构成的原电池中,若生成2gH2,则转移的电子数目为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com