
【题目】—定温度下,在三个等体积的恒容密闭容器中,反应2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g)达平衡,下列说法不正确的是( )
C2H5OH(g)+3H2O(g)达平衡,下列说法不正确的是( )
容器 | 温度/K | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | |||
CO2(g) | H2(g) | C2H5OH(g) | H2O(g) | C2H5OH(g) | ||
甲 | 500 | 0.20 | 0.60 | 0 | 0 | 0.083 |
乙 | 500 | 0.40 | 1.20 | 0 | 0 | |
丙 | 600 | 0 | 0 | 0.10 | 0.30 | 0.039 |
A. 该反应正反应为放热反应
B. 达平衡时,甲、乙容器内:2c(CO2,甲)>c(CO2,乙)
C. 达平衡时,容器甲中的逆反应速率比容器乙中的大
D. 达平衡时,转化率:a(CO2,甲)+a(C2H5OH,丙)>1
【答案】C
【解析】A.在容器甲和容器丙中,若温度一样,二者将建立完全相同的平衡。由表中数据可知,由于丙升高温度使C2H5OH(g)的平衡浓度减小,说明升温使化学平衡向逆反应移动,则正反应为放热反应,故A正确;B、乙容器中反应物浓度相当于在甲容器中等比例增大,若平衡不移动,则有2c(CO2,甲)=c(CO2,乙),但浓度等比例增大,相当于加压,该平衡向正反应移动,使c(CO2,乙)减小,所以有2c(CO2,甲)>c(CO2,乙),故B正确;C、由于容器乙中各物质的浓度比容器甲中的大,所以不论正逆反应速率,容器甲中反应速率都比容器乙中的小,故C错误;D、由A中的分析可知,当温度相同时,容器甲和容器丙将建立完全相同的平衡,即有a(CO2,甲)+a(C2H5OH,丙)=1,但容器丙由于升高温度,使平衡向逆反应方向移动,使a(C2H5OH,丙)转化率增大,所以a(CO2,甲)+a(C2H5OH,丙)>1,故D正确。所以本题正确选项为C。


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如右图所示。下列说法不正确的是
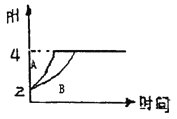
A. 图中表示醋酸溶液中pH变化曲线的是B
B. 设盐酸和醋酸中加入的Zn质量分别为m1、m2,则m1<m2
C. pH=2时盐酸和醋酸的物质的量前者小
D. pH=4时两溶液c(Zn2+)相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程中属于人工固氮的是( )
A.雷雨天气时产生少量NO
B.往农田中施放铵态氮肥
C.豆科植物等根部的根瘤菌吸收空气中的氮气转变为氨
D.N2和H2在高温、高压和催化剂存在下合成氨
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜在常温下能被稀硝酸溶解,其反应的化学方程式如下:3Cu + 8HNO3 (稀)=3Cu(NO3)2 + 2NO↑+ 4H2O。
(1)被氧化的元素是_______,被还原的元素是__________,发生氧化反应的物质是________,发生还原反应的物质是______________。
(2)用双线桥法表示反应电子得失的方向和数目:__________________________________。
(3)用单线桥法表示反应电子得失的方向和数目:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,分子数相同的是( )
A.2L SO2和2L CO2B.标准状况下1mol氧气和22.4L水
C.9g水和标准状况下11.2L CO2D.0.2molH2S和2.24LHCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)从氧化还原的角度分析水在下列化学反应中的作用(从氧化剂、还原剂角度分析)。
①电解水:_____________________________________________________。
②钠和水的反应(2Na+2H2O=2NaOH+H2↑):_______________________________。
③氟气和水反应(2F2+2H2O=4HF+O2):_______________________________。
④氯气和水反应(Cl2+H2O=HCl+HClO):______________________________。
(2)某一反应体系中有反应物和生成物共5种物质:S、H2S、HNO3、NO、H2O。该反应体系中还原产物是________;若反应中转移了0.3 mol电子,则氧化产物的质量是________g。
(3)将少量Cl2通入FeBr2的溶液中,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl,这个事实说明具有还原性的粒子还原性强弱顺序为____________。足量Cl2通入FeBr2溶液中发生反应的离子方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验需要0.2mol/L 的CuSO4溶液490mL,配制时应选用的容量瓶的规格和称取硫酸铜晶体(CuSO4·5H2O)的质量分别是( )
A.500mL 25gB.490mL 24.5g
C.490mL 25gD.500mL 24.5g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列图像的描述正确的是
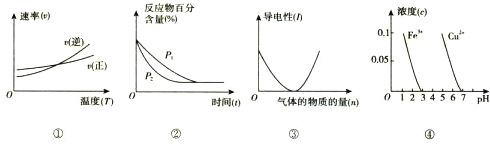
A. 根据图①判断反应A2(g)+3B2(g) ![]() 2AB3(g)的 △H>0
2AB3(g)的 △H>0
B. 图②可表示压强(P)对反应2A(g)+2B(g) ![]() 3C(g)+D(s)的影响
3C(g)+D(s)的影响
C. 图③可表示向醋酸溶液通入氨气时,溶液导电性随氨气量的变化
D. 根据图④,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com