
 HNO3�Ǽ�����Ҫ�Ļ���ԭ�ϣ���ҵ���Ʊ�HNO3����NH3�������������м������NO2���ܱ������ж��ѭ����ˮ�����Ʊ��ģ� �ݴ�����������⣺
HNO3�Ǽ�����Ҫ�Ļ���ԭ�ϣ���ҵ���Ʊ�HNO3����NH3�������������м������NO2���ܱ������ж��ѭ����ˮ�����Ʊ��ģ� �ݴ�����������⣺���� ��1�����������а�����2�������ã�һ���Ʊ����ᣬ��NԪ���غ�ɵù�ϵʽNH3��HNO3�����������ᷴӦ�õ�NH4NO3���ɷ���ʽ��֪ʵ�����õİ������������ʵ�����ȣ���������֮��Ϊ17��63���������淋�����������������立�Ӧ��ʵ�ʲμӷ�Ӧ�İ���������������ÿһ�������ʶ�ת��Ϊ��ʼԭ�������ʣ����������ᷴӦ�õ�NH4NO3ʱͶ�백�������������ݹ�ϵʽNH3��HNO3����ϳ���������а���������������֮��Ϊ��Ҫ������������
��2��������ʼʱNO2���ʵ���Ϊ1 mol������n��ѭ��������HNO3�����ʵ���Ϊ��Sn=$\frac{2}{3}$+$\frac{2}{3}$��$\frac{1}{3}$+$\frac{2}{3}$����$\frac{1}{3}$��2+$\frac{2}{3}$����$\frac{1}{3}$��3+??????+$\frac{2}{3}$����$\frac{1}{3}$��n-1�����ȱ�������Ϳɵã��ٸ���ת���ʹ�ʽ�����ת����a��ѭ������n֮���ϵ��
�ڸ��ݢ��еı���ʽ���㣻
��3���ٸ���ͼ���֪������Ũ�ȴ���10.0mol/Lʱ���������ֻ��NO2�����ݵ�ʧ�����غ��ԭ���غ�д������ʽ��
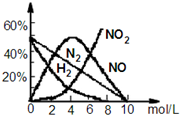
��960g Mg��1000L 4.0mol/L��HNO3��ַ�Ӧ��Mg�����ʵ����Ƚ��٣���Ӧ�������������ͼ���֪��n��NO����n��N2����n��NO2����n��H2��=5��3��1��1��ͬʱ��ԭ���ﻹ��NH4+������Mgʧȥ��������������õ�������֮����NH4+��������ͨ��ԭ���غ���ƽ���̣�
��� �⣺��1�����������а�����2�������ã�һ���Ʊ����ᣬ��NԪ���غ�ɵù�ϵʽNH3��HNO3�����������ᷴӦ�õ�NH4NO3���ɷ���ʽ��֪ʵ�����õİ������������ʵ�����ȣ���������֮��Ϊ17��63��
����80�ֵ������ʱ���μӷ�Ӧ����Ϊ80�֡�$\frac{17}{80}$=17�֣���Ҫ����Ϊ80��-17��=63�֣�
���Ʊ� 63t HNO3 ��ҪNH3������Ϊm����
NH3������������������������������HNO3
17 63
m��96%��92% 63 t
����17��63=m��96%��92%��63 t
���m=$\frac{17}{0.96��0.92}$ t��
����V��NH3��=[��$\frac{17}{0.96��0.92}$+17����106��17g/mol]��22.4L/mol=47.762��106L=47762m3��
�ʴ�Ϊ��47762��
��2��������ʼʱNO2���ʵ���Ϊ1 mol������n��ѭ��������HNO3�����ʵ���Ϊ��Sn=$\frac{2}{3}$+$\frac{2}{3}$��$\frac{1}{3}$+$\frac{2}{3}$����$\frac{1}{3}$��2+$\frac{2}{3}$����$\frac{1}{3}$��3+??????+$\frac{2}{3}$����$\frac{1}{3}$��n-1�����ȱ�������Ϳɵã�Sn=1-��$\frac{1}{3}$��n����NO2����HNO3ת����Ϊ��$\frac{1-��\frac{1}{3}��^{n}}{1}$=a����a=1-��$\frac{1}{3}$��n��
�ʴ�Ϊ��a=1-��$\frac{1}{3}$��n��
��n=1ʱ��ת����Ϊ66.7%
n=2ʱ��ת����Ϊ1-$\frac{1}{9}$=88.9%��96%
n=3ʱ��ת����Ϊ1-$\frac{1}{27}$=96.3%��96%
�ʾ���3��ѭ������������ʹ95%�Ķ�������ת��Ϊ���ᣬ
�ʴ�Ϊ��3��
��3���ٸ���ͼ���֪������Ũ�ȴ���10.0mol/Lʱ���������ֻ��NO2��Mg+HNO3��Mg��NO3��2+NO2��+H2O����Ӧ��HNO3��NO2��NԪ�ش�+5�۽���+4�۵õ�1�����ӣ�
Mg��Mg��NO3��2��MgԪ�ش�0������+2��ʧȥ2�����ӣ�����Mg�ļ�����Ϊ1��NO2�ļ�����Ϊ2���ٸ���ԭ���غ���ƽ��Mg+4HNO3=Mg��NO3��2+2NO2��+2H2O��
�ʴ�Ϊ��Mg+4HNO3=Mg��NO3��2+2NO2��+2H2O��
��960g Mg��1000L 4mol/L��HNO3��ַ�Ӧ��Mg�����ʵ���Ϊ40mol��HNO3�����ʵ���Ϊ4000mol����Ӧ�����������
��ͼ���֪��n��NO����n��N2����n��NO2����n��H2��=5��3��1��1��ͬʱ��ԭ���ﻹ��NH4+��
40 molMgʧȥ����Ϊ80 mol����Ӧ��������n=$\frac{224L}{22.4L/mol}$=10mol������n��NO��=10mol��$\frac{5}{10}$=5mol��nn��N2��=3mol��n��NO2��=1mol��n��H2��=1mol��������õ�������Ϊ5mol��3+3mol��5��2+1mol��1+1mol��2=48mol��
������NH4+ʱNԪ�صõ��ĵ���Ϊ80mol-48mol=32����������NH4+����Ϊ32��$\frac{1}{8}$=4mol��
����n��NO����n��N2����n��NO2����n��H2����n��NH4+����n��Mg��=5��3��1��1��4��40��
�ʷ�Ӧ����Ϊ��40Mg+100 HNO3=5NO��+3N2��+H2��+NO2��+4NH4NO3+40Mg��NO3��2+41H2O��
�ʴ�Ϊ��40Mg+100 HNO3=5NO��+3N2��+H2��+NO2��+4NH4NO3+40Mg��NO3��2+41H2O��
���� ���⿼�黯ѧ���㣬��Ŀ���������̸��ӣ������״���Ŀ�����ؿ���ѧ�����������������ѶȱȽϴ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ǽ���Ԫ��R���γɵĺ������Σ�MaROb���е�RԪ�رض��������� | |
| B�� | ֻ�зǽ���Ԫ�ز����γɺ������� | |
| C�� | ����Ԫ���еĽ���Ԫ���γɵ����������һ������һ����ϡ������Ԫ�ص�ԭ�Ӻ�������Ų���ͬ | |
| D�� | �ǽ���Ԫ�ص���ۺ����ᶼ����ǿ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ȳ���ӵ����ģ�ͣ� | B�� | �ǻ��ĵ���ʽ��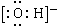 | ||
| C�� | 2�ȱ���Ľṹ��ʽ��CH3CHClCH3 | D�� | ��ϩ�ļ���ʽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ŵ�ʱ��������Fe������ԭ��Ӧ | |
| B�� | �ŵ�ʱ��������Ӧ�ǣ�NiO2+2e-+2H+=Ni��OH��2 | |
| C�� | �ŵ�ʱ��Ni��OH��2�ǻ�ԭ���� | |
| D�� | �����طŵ���̺ͳ����̷������ǿ��淴Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Q��Q1��2Q2 | B�� | Q2��Q1��2Q2 | C�� | Q=Q1��Q2 | D�� | Q1=2Q2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2���ӵĽṹʽ��O=C=O | B�� | NaCl�ĵ���ʽ��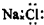 | ||
| C�� | N2�Ľṹʽ��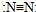 | D�� | F��ԭ�ӽṹʾ��ͼ��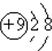 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3 | B�� | 4 | C�� | 5 | D�� | 6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8�� | B�� | 7�� | C�� | 6�� | D�� | 5�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һ����ˮ�������c��H+��=10-amol/L | |
| B�� | ��ˮϡ�ͣ������Ƶ�ˮ��̶�����ˮ�ĵ���̶�Ҳ���� | |
| C�� | �������ᣬpH=7ʱ����c��Cl-��=c��CH3COOH�� | |
| D�� | ����Һ�м����������ԣ���һ����c��CH3COO-����c��Na+����c��H+����c��OH-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com