
已知烯烃、炔烃在臭氧的作用下发生以下反应:
CH3—CH===CH—CH2—CH===CH2→CH3CHO+OHC—CH2—CHO+HCHO
CH3—C≡C—CH2—C≡CH―→CH3COOH+HOOCCH2COOH+HCOOH 某烃分子式为C10H10,在臭氧作用下发生反应:C10H10→CH3COOH+3HOOC—CHO+CH3CHO,下列判断正确在是:( )
A.其结构中含有4个碳碳双键,4个碳碳三键
B.分子中含有4个碳碳双键和2个碳碳三键
C.该烃结构简式是:CH3-C≡C-CH=CH-C≡C-CH=CH-CH3
D. 其结构中含有2个碳碳双键,4个碳碳三键
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
放射性元素钚(Pu)有20种放射性同位素,下列关于 Pu和
Pu和 Pu的说法正确的是( )
Pu的说法正确的是( )
A. Pu和
Pu和 Pu都含有94个中子
Pu都含有94个中子
B. Pu和
Pu和 Pu互为同位素
Pu互为同位素
C. Pu和
Pu和 Pu的核外电子数不同
Pu的核外电子数不同
D. Pu和
Pu和 Pu分别含有146和147个质子
Pu分别含有146和147个质子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质性质递变正确的是( )
A.原子半径:C、Al、K依次增大
B.热稳定性:HF、NH3、SiH4依次增强
C.水化物的酸碱性:NaOH、Al(OH)3、Mg(OH)2碱性减弱
D.非金属性:Cl、P、S依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
锌与很稀的硝酸溶液反应的化学方程式为:
4Zn +10HNO3== 4Zn(NO3)2 + NH4NO3 + 3H2O,按要求回答下列问题:(共10分)
(1)该反应中HNO3表现的化学性质是 。(填序号)
① 只有酸性 ② 只有氧化性 ③ 只有还原性 ④酸性与还原性 ⑤ 酸性与氧化性
(2)现有13.0 g 锌与足量的稀硝酸发生上述反应,则反应过程中转移的电子物质的量是多少?被还原的HNO3物质的量是多少?(写出规范的计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
常温常压下,50mL三种气态烃按任意比例混合,与足量氧气混合后点燃爆炸,恢复到原来状况时,体积共缩小100mL,则三种烃可能是( )
A.CH4 C2H4 C3H4 B.C2H6 C3H6 C4H6 C.CH4 C2H6 C3H8 D.C2H2 C2H6 C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组在实验室用如图所示装置探究氮氧化物气体与烧碱溶液的反应。实验过程中将胶头滴管中的液体挤入烧瓶,若碱液可快速、充分吸收产生的氮氧化物气体。下列叙述正确的是( )
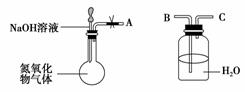
A.若将A与B连接,打开止水夹,则广口瓶中长导管口有气泡产生
B.若将A与C连接,打开止水夹,水沿导管由广口瓶进入烧瓶中
C.无论A连接B还是C,打开止水夹,均无明显现象
D.若将NaOH溶液换为水,可以用这套装置验证氨气易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
中华人民共和国国家标准(GB27602011)规定葡萄酒中SO2最大使用量为0.25 g·L-1。某兴趣小组用题图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
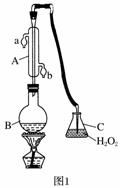
(1)仪器A的名称是______________,水通入A的进口为________。
(2)B中加入300.00 mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为________________________________。
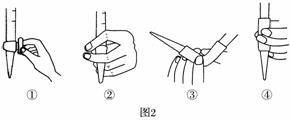
(3)除去C中过量的H2O2,然后用0.090 0 mol·L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择题图2中的________;若滴定终点时溶液的pH=8.8,则选择的指示剂为________;若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号)________(①=10 mL,②=40 mL,③<10 mL,④>40 mL)。
(4)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中SO2含量为________g·L-1。
(5)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com