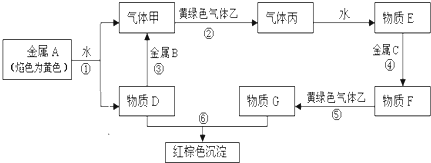
解:金属A焰色反应为红色,故A为金属Na,乙是黄绿色气体,乙为Cl
2,H为红褐色沉淀,为Fe(OH)
3;
由反应①Na→气体甲+D,考虑Na与水的反应,故甲为H
2,D为NaOH,由NaOH+金属B→H
2可知,B为金属Al,由甲+乙→丙,故丙为HCl,HCl溶于水的物质E,故E为盐酸;
G+NaOH→Fe(OH)
3,G含有Fe
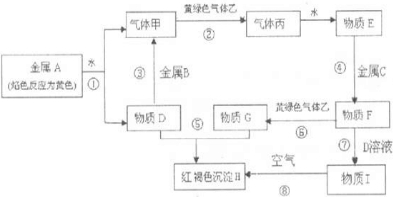
3+,由E(盐酸)
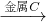
F
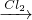
G可知,C为Fe,F为FeCl
2,G为FeCl
3;
(1)由上述分析可知,A为Na,B为Al,C为Fe,故答案为:Na;Al;Fe;
(2)反应③是铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH
-+2H
2O═2AlO
2-+3H
2↑;
反应⑥是氯化亚铁与氯气反应生成氯化铁,反应离子方程式为:2Fe
2++Cl
2═2Fe
3++2Cl
-,
故答案为:2Al+2OH
-+2H
2O═2AlO
2-+3H
2↑;2Fe
2++Cl
2═2Fe
3++2Cl
-;
(3)F为FeCl
2,检验FeCl
2溶液中Fe
2+的方法是:取少量溶液于试管中,滴加KSCN溶液无明显现象,再滴加新制氯水,溶液变红,
故答案为:取少量溶液于试管中,滴加KSCN溶液无明显现象,再滴加新制氯水,溶液变红.
分析:金属A焰色反应为红色,故A为金属Na,乙是黄绿色气体,乙为Cl
2,H为红褐色沉淀,为Fe(OH)
3;
由反应①Na→气体甲+D,考虑Na与水的反应,故甲为H
2,D为NaOH,由NaOH+金属B→H
2可知,B为金属Al,由甲+乙→丙,故丙为HCl,HCl溶于水的物质E,故E为盐酸;
G+NaOH→Fe(OH)
3,G含有Fe
3+,由E(盐酸)
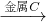
F
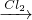
G可知,C为Fe,F为FeCl
2,G为FeCl
3.
点评:本题以无机框图题的形式考查Na、Al、Fe、Cl等元素单质及其化合物之间的相互转化关系、化学用语的书写、离子检验等,难度中等,注意基础知识的掌握.

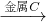 F
F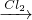 G可知,C为Fe,F为FeCl2,G为FeCl3;
G可知,C为Fe,F为FeCl2,G为FeCl3;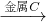 F
F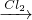 G可知,C为Fe,F为FeCl2,G为FeCl3.
G可知,C为Fe,F为FeCl2,G为FeCl3.

 阅读快车系列答案
阅读快车系列答案