
| A. | “膏液”的主要成分是石油 | B. | “膏液”是天然高分子化合物 | ||
| C. | “膏液”是烃的混合物 | D. | “膏液”能发生取代反应 |
分析 依据:草木之实,其中蕴藏膏液而不能自流,可知“膏液”应为植物果实种子压榨出的植物油,依据植物油的性质判断解答.
解答 解:依据:草木之实,其中蕴藏膏液而不能自流,可知“膏液”应为植物果实种子压榨出的植物油,植物油属于油脂,油脂是由高级脂肪酸和甘油反应生成的酯,
A.“膏液”的主要成分是植物油,故A错误;
B.“膏液”的主要成分是植物油,植物油不是高分子化合物,故B错误;
C.“膏液”的主要成分是植物油,属于酯,不含烃,故C错误;
D.“膏液”的主要成分是植物油,植物油属于油脂,油脂是由高级脂肪酸和甘油反应生成的酯,酯能够发生水解,水解属于取代反应,故D正确;
故选:D.
点评 本题考查了油脂的结构及性质,准确把握题意,明确油脂的结构及性质即可解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
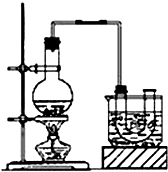 已知:CH3CH2OH+NaBr+H2SO4(浓)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.
已知:CH3CH2OH+NaBr+H2SO4(浓)$\stackrel{△}{→}$ CH3CH2Br+NaHSO4+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.4g | B. | 6g | C. | 12.4g | D. | 8.8g |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
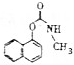 )在农业上可应用于防治稻飞虱、叶蝉、蓟马、豆蚜、大豆食心虫、棉铃虫及果树害虫、林业害虫等.下面是用萘酚(
)在农业上可应用于防治稻飞虱、叶蝉、蓟马、豆蚜、大豆食心虫、棉铃虫及果树害虫、林业害虫等.下面是用萘酚(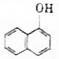 )合成西维因的反应:
)合成西维因的反应: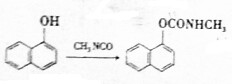
| A. | 该反应为加成反应 | |
| B. | 可用FeCl3溶液检验萘酚是否完全反应 | |
| C. | 萘酚与苯酚互为同系物 | |
| D. | 1mol西维因最多能与2molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上10月月考化学试卷(解析版) 题型:填空题
汽车常装有安全气囊,当发生强烈碰撞时,瞬间引发以下反应:2NaN3=2Na+3N2↑,所产生的气体快速充满气囊,可以达到保护车内人员的目的.
(1)若气囊中装有130g NaN3,则其物质的量是_______________.
(2)若130g NaN3完全分解,在标准状况下,气囊膨胀的体积约为_______________.
(3)该反应中的氧化剂是 氧化产物是__________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省高一上10月月考化学试卷(解析版) 题型:选择题
混合气体由CH4和N2组成,测得混合气体在标准状况下的密度为0.893g/L,则混合气体中N2和CH4的体积之 比为
比为
A.1:2 B.1:4 C.2:1 D.4:1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上第一次月考化学试卷(解析版) 题型:填空题
I.某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
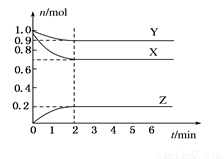
(1)该反应的化学方程式为_______________________。
(2)反应开始至2 min,气体Z的平均反应速率为____________。
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的____________倍;
②若此时将容器的体积缩小为原来的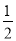 倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为____________反应(填“放热”或“吸热”)。
倍,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为____________反应(填“放热”或“吸热”)。
Ⅱ.某科研小组欲研究在其他条件不变的情况下,改变起始氧气的物质的量对合成新型硝化剂反应:4NO2(g)+O2(g) 2N2O5(g) ΔH<0的影响。
2N2O5(g) ΔH<0的影响。

(1)图像中T1和T2的关系是T1________T2(填“>”、“<”或“=”);
(2)比较a、b、c三点所处的平衡状态中,反应物NO2的转化率最大的是__________(填字母);
(3)若容器体积为1 L,n=1 mol,NO2的转化率为50%,则此条件下(T2),反应的平衡常数K=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com