
����Ŀ�����ſ�ѧ�����ķ�չ�������ӵ������IJⶨ�ֶ�Խ��Խ�࣬�ⶨ��ȷ��ҲԽ��Խ�ߣ�����һ�ּ��еIJⶨ���������岽��Ϊ��
(1)������NaCl��ϸ�������ȷ��ȡmgNaCl���岢ת�Ƶ���������A�С�
(2)�õζ�����A�����еμӱ��������������ӱ���A�����Ŀ̶��ߣ������NaCl��������ΪVcm3��
�ٲ���(1)��A���������__________���������ƣ���
�ڲ���(2)������ʽ�ζ��ܺû��Ǽ�ʽ�ζ��ܺã�__________��������______________��
���ܷ��ý�ͷ�ιܴ��沽��(2)�еĵζ���__________��������____________________��
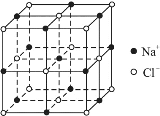
����֪NaCl����Ľṹ����ͼ��ʾ����X���߲��NaCl�����п��������Na+��Cl-���ƽ������Ϊacm�����������ⶨ������ð����ӵ�����NA�ı���ʽΪ��NA=______mol-1��
���𰸡�����ƿ ��ʽ�ζ��� �����ܽ��ʽ�ζ��ܵ���Ƥ�� ���� ʵ������Ҫȷ��ȡ������� ![]()
��������
������ƿΪ�����������ܹ���ȷ�IJⶨ�����
�ڱ�Ӧ����ʽ�ζ���ʢװ�����ܸ�ʴ��ʽ�ζ��ܵ���Ƥ�ܣ�
��ʵ������Ҫȷ��ȡ�����������˲����ý�ͷ�ιܴ���ζ��ܣ�
����ʵ����NaCl����������������Եõ�NaCl������ܶȣ���̯�����㾧����Na+��Cl-��Ŀ���ð���٤��������ʾ�����������������Na+��Cl-���ƽ������Ϊacm�����ⳤ=2acm���������������ھ����ܶ��뾧������˻����������㡣
���ܹ���ȷ�IJⶨNaCl������������Բ���(1)���������������ƿ��
�����ڱ����������͡��ϻ����ã����Եζ�������ʽ�ζ��ܣ�
��ʵ������Ҫȷ��ȡ�����������˲����ý�ͷ�ιܴ���ζ��ܣ�
��NaCl���ܶ�Ϊ��=![]() g/cm3�������Na+��Cl-���ƽ������Ϊacm�����ⳤ=2acm��NaCl���������=(2a)3cm3��������Na+������Ŀ=1+12��
g/cm3�������Na+��Cl-���ƽ������Ϊacm�����ⳤ=2acm��NaCl���������=(2a)3cm3��������Na+������Ŀ=1+12��![]() ��Cl-��Ŀ=8��
��Cl-��Ŀ=8��![]() +6��
+6��![]() =4����NaCl����������=
=4����NaCl����������=![]() g=
g=![]() g/cm3��(2a)3cm3�������ɵ�NA=
g/cm3��(2a)3cm3�������ɵ�NA=![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ��������ѧ������չʷ�ϵ�һ���ش�ͻ�ƣ��о�����Һ����һ�����õĴ������ʡ�
(1)N2(g)+3H2(g)2NH3(g) ��H��0���о��������������ɼ��ٰ����ĺϳɡ��±�Ϊij�¶��µ������IJ�ͬ�����ֱ���ϳɰ���ʱ�������ij�ʼ����(mmol min-1)��
���� | Ru | Rh | Ni | Pt | Pd | Fe |
��ʼ���� | 7.9 | 4.0 | 3.0 | 2.2 | 1.8 | 0.5 |
�ٲ�ͬ���������£��ϳɰ�����Ӧ�Ļ��������_______ (��д�����Ļ�ѧʽ)��
��ij�о�С���һ��̽�������Ժϳɰ�����Ӱ�졣��N2��H2��һ��������ͨ�����ֲ�ͬ�Ĵ������з�Ӧ����ͬʱ���ڲ����ݳ�������NH3����������ͼ���Ӷ�ȷ���¶ȶԴ�����Ӱ�졣a��___ (��ǡ����ǡ�)��Ӧ�¶��°���ƽ��ʱ�İٷֺ�����˵��������___��

(2)�����ķֽⷴӦ2NH3N2+3H2 ��H��0������ʵ��������������������ͬʱͨ�백����ˮ���������������ѹ�Ͱ���ת������ʱ��仯�����ͼ��ʾ��
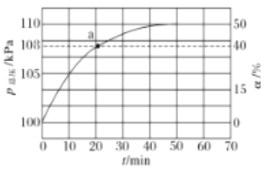
��ƽ��ʱ��p(H2O)= ___kPa��ƽ�ⳣ��Kp=_____KPa2(KpΪ�Է�ѹ��ʾ��ƽ�ⳣ��)��
�ڷ�Ӧ����v=v��-v��=K��p2(NH3)-K��p(N2)p3(H2)��k����k���ֱ�Ϊ�����淴Ӧ���ʳ���������a����![]() =__��
=__��
(3)Һ���У�2NH3(l)NH2-+NH4+����Pt�缫��Һ�����е��Ҳ�ɲ���H2��N2�������ĵ缫��Ӧ______��
(4)���������ð�ˮ����SO2������SO2������ͨ��ð�ˮ�У�����Һ������ʱ����Һ�е�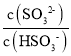 =____��(��֪25�棬Kb(NH3H2O)=1.810-5��Ka1(H2SO3)=.310-2��Ka2(H2SO3)=6.210-8)
=____��(��֪25�棬Kb(NH3H2O)=1.810-5��Ka1(H2SO3)=.310-2��Ka2(H2SO3)=6.210-8)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�������Դ����������ȡ������һֱ������Դ����������о��ȵ㡣
��1����ҵ����ȡ![]() �ж��ַ������磺
�ж��ַ������磺
��![]()
��![]()
��![]()
�����ˮ�����������Ƹߴ���ʱ����ʼ��Ӧ��������Ϊ![]() ��
��![]() �������ʵ���֮��Ϊ4��1����÷�Ӧ���Ȼ�ѧ����ʽΪ________��
�������ʵ���֮��Ϊ4��1����÷�Ӧ���Ȼ�ѧ����ʽΪ________��
��2�������Ͻ���һ�����õĴ�����ϣ�������㶨���ܱ������г��������������·�Ӧ��![]() ��
��![]() ��ƽ��ת���������ʼ�������ʵ���
��ƽ��ת���������ʼ�������ʵ���![]() ����Ӧ�¶�
����Ӧ�¶�![]() �Ĺ�ϵ����ͼ��ʾ��һ���¶��£������ڵ�ѹǿ
�Ĺ�ϵ����ͼ��ʾ��һ���¶��£������ڵ�ѹǿ![]() ��ʱ��
��ʱ��![]() �ı仯��ϵ����ͼ��ʾ��
�ı仯��ϵ����ͼ��ʾ��
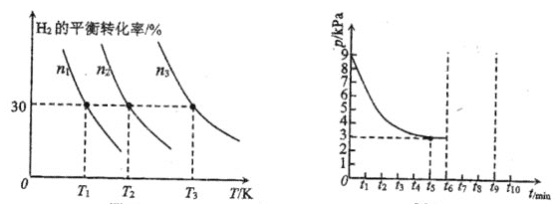
����ͼ��![]() ��ʼ�������ɴ�С����________��
��ʼ�������ɴ�С����________��
�ڸ÷�Ӧƽ�ⳣ���Ĵ�С��ϵΪ![]() ________
________![]() ����
����![]() ����
����![]() ������
������![]() ��
��![]() ��������________��
��������________��
���������¶Ȳ��䣬��![]() ʱ�̽��������ݻ�ѹ����ԭ����һ�룬����
ʱ�̽��������ݻ�ѹ����ԭ����һ�룬����![]() ʱ�̴ﵽƽ�⡣������ͼ�л�����Ӧ�ı仯����______��
ʱ�̴ﵽƽ�⡣������ͼ�л�����Ӧ�ı仯����______��
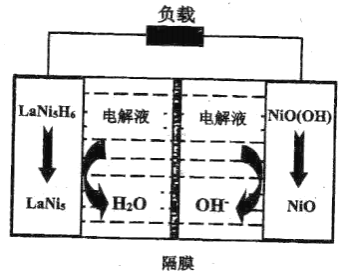
��ij���������طŵ�ʱ�Ĺ���ԭ����ͼ��ʾ�����и�ĤΪ________���ӽ���Ĥ![]() ����������������
����������������![]() �������ĵ缫��ӦʽΪ________��
�������ĵ缫��ӦʽΪ________��
��3��������Խ����л�������û�����ͱ�֮��Ŀ��淴Ӧ��ʵ������ͼ��⣺
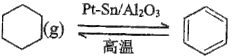
![]() ����ij�¶��£����ݻ�Ϊ2L�ĺ��������м���
����ij�¶��£����ݻ�Ϊ2L�ĺ��������м���![]() �����飬ƽ��ʱ��ϵ��ѹǿΪ
�����飬ƽ��ʱ��ϵ��ѹǿΪ![]() ���������ʵ���Ϊ
���������ʵ���Ϊ![]() ����ƽ�ⳣ��
����ƽ�ⳣ��![]() ________
________![]() �ú�a��b��p�Ĵ���ʽ��ʾ����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ
�ú�a��b��p�Ĵ���ʽ��ʾ����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ![]() ��ѹ
��ѹ![]() ���ʵ�������
���ʵ�������![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС����ϡ����ߴ���п������ͼ��ʾװ����ȡH2����ԭCuOʱ������β�����д̼��ԡ�ͨ����һ��̽����֤��β���к���SO2��
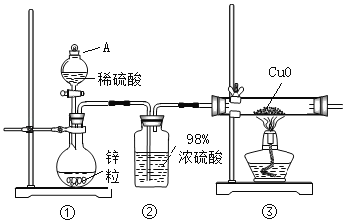
(1)Aװ�õ�����_____����װ����Ũ���������_____��
(2)�����ۣ���ΪSO2�IJ������������ֿ��ܣ�
��ͬѧ��_____��Ӧ������SO2��
��ͬѧ��H2���װ����Ũ���ᷴӦ������SO2��
�����Ƽ�ͬѧ�IJ��룬����Ϲ�ѡ�Լ���Ƽ�����֤��ͬѧ����ĺ����ԡ�(������ѡ���������Լ��⣬����ѡ�Լ����£�ϡ���ᡢϡ���ᡢ��ˮ�Ȼ��ơ���ʯ��)________________________
(3)�����ͬѧ������������û�ѧ����ʽ��ʾ��ԭ��_____��
(4)��֪������H2���������Ը��������Һ��Ӧ����ͬѧ��������ڢ�װ��ǰ�����Ը��������Һ��ȥSO2���������ӷ���ʽ��ʾ��Ӧ��ԭ����_____��
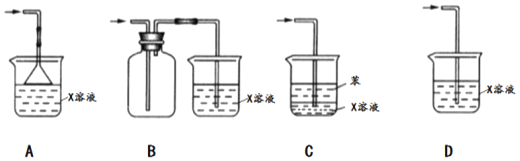
(5)SO2��һ���ж�����Ⱦ�����壬ʵ���ҳ���X��Һ����β��������X��_____(�ѧʽ)��β������ʱ����װ�ò���������Ч������_____(��ѡ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ָ����Ӧ�����ӷ���ʽ��ȷ����(����)
A.��ʯī���缫���MgCl2��Һ��2H2O��2Cl��![]() 2OH����H2����Cl2��
2OH����H2����Cl2��
B.��������������ϡ���Fe��4H����NO3-=Fe3����NO����2H2O
C.��Na2S2O3��Һ����ˮ�е�Cl2��4Cl2��S2O32-��5H2O=10H����2SO42-��8Cl��
D.SO2ͨ��FeCl3��Һ�У�SO2��Fe3����2H2O=SO42-��Fe2����4H��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������С�ظ���Ԫ(Ҳ�ƾ���)�����������壬�����������8���������һ����ԭ�ӣ��������������һ����ԭ�ӣ�ÿ����ԭ�ӱ����ڵľ������á���ԭ�ӵ�ֱ��Ϊdcm����NA��ʾ�����ӵ�������M��ʾ���Ħ������(��λ��g��mol��1)��
(1)����ÿ�������к���________����ԭ�ӡ�
(2)������һ����������������ٶ���ԭ���Ǹ���С���⣬��Ӧ�ٶ�_________��
(3)һ�����������Ϊ________cm3��
(4)������ܶ�Ϊ________g��cm��3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������(K2FeO4)��һ��������ɫ����������������(����������ԭ��Ӧ)����γ�Fe(OH)3���壬�����ڴ�������ˮ����ҵ���иɷ���ʪ�������Ʊ�������صķ�����
(1)�ɷ��Ʊ��������ʱ�����Ʊ��õ�Na2FeO4����ӦΪ��2FeSO4��6Na2O2=2Na2FeO4��2Na2O��2Na2SO4��O2��
�ٸ÷�Ӧ�У���������________������������________��
��ÿ����1 mol Na2FeO4��ת��________mol���ӡ�
(2)��ƽʪ���Ʊ�������ط�Ӧ�����ӷ���ʽ��______Fe(OH)3��______ClO����______OH��=______FeO42����______Cl����______H2O
(3)ȡ����K2FeO4��Һ���μ����ᣬ��Cl2�������÷�Ӧ���������ԣ�K2FeO4______(����>������<��)Cl2��
(4)Fe(OH)3�����ʹˮ�����������������������ˮ����ʵ�����ñ����Ȼ�����Һ��ȡFe(OH)3����Ļ�ѧ����ʽ��_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧ�����ǻ�ѧ��Ӧԭ������Ҫ��ɲ��֡���ش��������⣺
��1����֪һ�������·�����Ӧ��2SO2��g��+O2��g��![]() 2SO3��g����H��0���ڷ�Ӧ�����У�����Ӧ���ʵı仯��ͼ��ʾ����������ʵı仯�ش��ȡ�Ĵ�ʩ���ı����������
2SO3��g����H��0���ڷ�Ӧ�����У�����Ӧ���ʵı仯��ͼ��ʾ����������ʵı仯�ش��ȡ�Ĵ�ʩ���ı����������
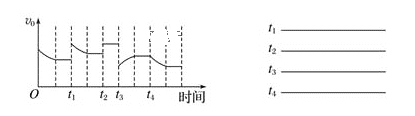
_______��________��_______��______
��2��̽����Ӧ������0.l0 mol��L-1Na2S2O3��Һ��ϡH2SO4��Ӧ���ʵ�Ӱ�졣�������ⶨ��������
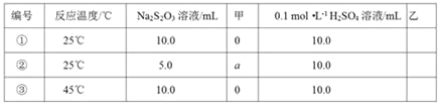
����ʵ��٢���̽��____�Ի�ѧ��Ӧ���ʵ�Ӱ�죻������ʵ��٢���̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬�������������Ϊ____��aΪ____������ʵ����Ҫ���������������������������Ϊ____��
��3����֪2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2�����ڿ�ʼһ��ʱ���ڣ���Ӧ���ʽ�С����Һ��ɫ�����ԣ�������ͻȻ��ɫ����Ӧ������������
�������������ijͬѧ��Ϊ�÷�Ӧ���ȣ�������Һ�¶���������Ӧ��������Ӱ�컯ѧ��Ӧ���ʵ����ؿ�������뻹������___��Ӱ�졣
������ʵ��֤����IJ��룬�����Ը��������Һ��������Һ�⣬�����ڷ�Ӧһ��ʼʱ����____������ĸ����
A������� B���Ȼ��� C�������� D��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������茶���[(NH4)2Fe(SO4)2��6H2O]��һ���ȶ��Ļ�ԭ����������������ѧ�еĵζ�����ij������������з����Ʊ��þ��壬���������ȶ��Խ���������ʵ�顣
��.��������茶�����Ʊ�:
����![]() FeSO4��Һ
FeSO4��Һ![]() �ᾧ
�ᾧ![]() ��������茶���
��������茶���
(1)����Ũ�ȹ���Ӧ����ͬʱ��ʹFeSO4��Һ�л���_____________(�����ӷ���)��
(2)����FeSO4��Һ��(NH4)2SO4�����Ʊ��þ���Ļ�ѧ����ʽ_____________��
��.��������茶�����ȷֽ����̽��:��С��ͬѧѡ����ͼ��ʾ����װ�ý���ʵ��(�г�װ����)����������:��������������500���������������ȫ�ֽ⣬�����к�����������������������ˮ�����ȡ�
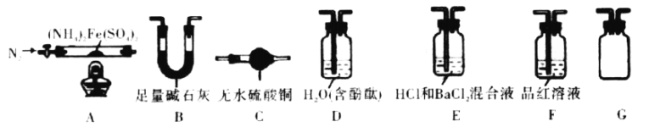
(3)��ȼA���ľƾ���֮ǰ���ȴ��ɼУ�ͨһ��ʱ��N2����Ŀ����____________��
(4)ѡ���������ֱ�Ҫ��װ�����������Ӧʵ�飬��д�����ϵ����ݡ�
������ܲ��� | װ������˳�� | װ������ | ʵ������ | ʵ����� |
H2O��NH3 | ACBGD | ��B������______ | ��C��________�� D��__________�� | ��H2O��NH3 |
SO2��SO3 | ��___________ | ��E��HCl������ ___________ | E��û����������F����Һ��ɫ | ��___________ |
(5)Ϊ֤���ȷֽ���ȫ������Ĺ����ΪFe2O3��������FeO��Fe3O4����Ҫѡ�õ��Լ���__________(ѡ������ĸ)������������ѡ�Լ�����ʵ��֤���ķ���____________��
A.ϡ���� B.ϡ���� C.KSCN��Һ D.H2O2��Һ E.K3[Fe(CN)6]��Һ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com