
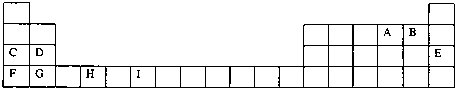
���� ��Ԫ�������ڱ���λ�ÿ�֪��A��I�ֱ�ΪO��F��Na��Mg��Ar��K��Ca��Ti��Cr��
��1��Ԫ��IΪ����M2+����3d�������6�����ӣ�M�ļ۵���Ϊ3d64s2����ԭ������Ϊ18+2+6=26��ΪFeԪ�أ�
��2����������ǿ����һ��������С���ǽ�����Խǿ���縺��Խ��ϡ��������������ȶ���
��3���������d�����d����
��4��F�Ľ����Ա�Cǿ�������ý�����ˮ��Ӧ�ľ��ҳ̶�˵����
��� �⣺��Ԫ�������ڱ���λ�ÿ�֪��A��I�ֱ�ΪO��F��Na��Mg��Ar��K��Ca��Ti��Cr��
��1��Ԫ��IΪCr��M2+����3d�������6�����ӣ�M�ļ۵���Ϊ3d64s2����ԭ������Ϊ18+2+6=26��ΪFeԪ�أ�λ�����ڱ���������VIB�壬
�ʴ�Ϊ��Cr���ģ�VIB��
��2��K�Ľ�������ǿ����һ��������С��F�ķǽ�����Խǿ���縺��Խ��ϡ��������������ȶ�����Ar�Ļ�ѧ�������ȶ���
�ʴ�Ϊ��K��F��Ar��
��3���������d����λ��d������֪Ԫ�ش���d������Ti��Cr���ʴ�Ϊ��Ti��Cr��
��4��F�Ľ����Ա�Cǿ����ͬ�����£���ˮ��Ӧ�ر��ƾ��ң��������صļ��Ա���������ǿ������ԭ�ӽṹ���۽�����ԭ��Ϊ�ص�ԭ�Ӱ뾶���ƴ�ԭ�Ӻ˶��������ӵ��������������Ƚ�����ʧ���ӣ�
�ʴ�Ϊ����ͬ�����£���ˮ��Ӧ�ر��ƾ��ң��������صļ��Ա���������ǿ�����ص�ԭ�Ӱ뾶���ƴ�ԭ�Ӻ˶��������ӵ��������������Ƚ�����ʧ���ӣ�
���� ���⿼��λ�á��ṹ�����ʵĹ�ϵ��Ϊ��Ƶ���㣬����Ԫ�ص�λ�á����ʼ��ṹ������Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬��Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
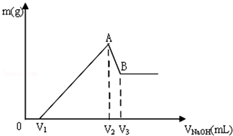 ��Mg��Al��ɵĻ���ﹲ0.1mol����100mL 3mol/LHCl��Һ�У��ٵμ�1mol/LNaOH ��Һ���ڵμ�NaOH��Һ�Ĺ����У�����������m��NaOH��Һ���V�ı仯��ͼ��ʾ��
��Mg��Al��ɵĻ���ﹲ0.1mol����100mL 3mol/LHCl��Һ�У��ٵμ�1mol/LNaOH ��Һ���ڵμ�NaOH��Һ�Ĺ����У�����������m��NaOH��Һ���V�ı仯��ͼ��ʾ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �ڢ� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
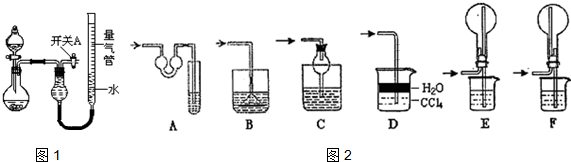
| ʵ�� | ҩƷ | ��ȡ���� | �������е�Һ�� |
| �� | Cu��ϡHNO3 | H2O | |
| �� | NaOH���塢Ũ��ˮ | NH3 | |
| �� | Na2SO3���塢ŨH2SO4 | SO2 | |
| �� | þ���Ͻ�NaOH��Һ�������� | H2 | H2O |
| ��� | þ���Ͻ���� | �����ܵ�һ�ζ��� | �����ܵڶ��ζ��� |
| �� | 1.0g | 10.0mL | 346.3mL |
| �� | 1.0g | 10.0mL | 335.0mL |
| �� | 1.0g | 10.0mL | 345.7mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
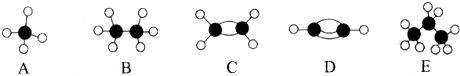
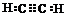 ��A�Ķ���ȡ������1�֣�
��A�Ķ���ȡ������1�֣��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2��SiO2��CO��Ϊ���������� | B�� | ϡ���������ᡢ�Ȼ�����Һ��Ϊ���� | ||
| C�� | �ռ���ʯӢ��Ϊ����� | D�� | ��ˮ��ˮ��������ˮ��Ϊ����� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com