
| A. | Si→SiO2→H2SiO3→Na2SiO3 | |
| B. | Al→Al2O3→Al(OH)3→NaAlO2 | |
| C. | Na→Na2O→Na2O2→NaOH→Na2CO3→NaHCO3 | |
| D. | S→SO3→H2SO4→SO2→Na2SO3→Na2SO4 |
分析 A.二氧化硅不溶于水,不会与水反应生成硅酸;
B.氧化铝不溶于水,则氧化铝不会一步反应生成氢氧化铝;
C.钠与氧气在常温下生成氧化钠,氧化钠加热生成过氧化钠,过氧化钠与水反应生成氢氧化钠,氢氧化钠与二氧化碳生成碳酸钠,碳酸钠与二氧化碳反应生成碳酸氢钠;
D.S与氧气反应生成的是二氧化硫,不会生成三氧化硫.
解答 解:A.SiO2不与水反应,则SiO2→H2SiO3不会一步实现,故A错误;
B.Al2O3不溶于水,则Al2O3不会与水一步反应生成Al(OH)3,故B错误;
C.钠性质较活泼,在不加热条件下与氧气反应生成氧化钠,氧化钠与氧气加热生成过氧化钠,过氧化钠与水反应生成氢氧化钠,氢氧化钠与二氧化碳生成碳酸钠,碳酸钠与二氧化碳反应生成碳酸氢钠,所以转化关系Na→Na2O→Na2O2→NaOH→Na2CO3→NaHCO3都可一步实现,故C正确;
D.S与氧气反应生成SO2,所以S→SO3不会一步实现,故D错误;
故选C.
点评 本题考查了常见元素单质及其化合物性质,题目难度中等,明确常见元素及其化合物性质为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强电解质一定是离子化合物,弱电解质一定是共价化合物 | |
| B. | 强电解质一定是易溶化合物,弱电解质一定是难溶化合物 | |
| C. | SO3溶于水后水溶液导电性很强,所以SO3是强电解质 | |
| D. | 强电解质与弱电解质的本质区别是在水溶液中能否完全电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
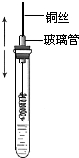 某同学在学习乙醇的知识后,设计了如下的实验. 操作步骤为:
某同学在学习乙醇的知识后,设计了如下的实验. 操作步骤为:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
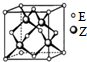 X、Y、Z、R、W、E为前四周期元素且原子序数依次增大.X的单质与Y的单质在放电条件下反应产生大气污染物,R基态原子的M能层上有3对成对电子,W核外有5个未成对电子.Y、Z分别形成氢化物Q和J,已知Q与J摩尔质量相等,Q的水溶液中加入少量WY2,立即产生大量气泡.E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:
X、Y、Z、R、W、E为前四周期元素且原子序数依次增大.X的单质与Y的单质在放电条件下反应产生大气污染物,R基态原子的M能层上有3对成对电子,W核外有5个未成对电子.Y、Z分别形成氢化物Q和J,已知Q与J摩尔质量相等,Q的水溶液中加入少量WY2,立即产生大量气泡.E位于周期表的ds区,最外层只有一对成对电子.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定含有I-,不能确定是否含有Cl- | B. | 一定含有NO3- | ||
| C. | 不含有Fe3+,可能含有NO3- | D. | 一定含有I-、NO3-和Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第三周期ⅣA族 | B. | 第三周期ⅢA族 | C. | 第四周期ⅣA族 | D. | 第四周期ⅣB族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com