
| A. | v(B2)=0.8 mol/(L•s) | B. | v(B2)=3mol/(L•min) | C. | v(C)=0.6 mol/(L•s) | D. | v(A2)=0.4 mol/(L•s) |
分析 不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与化学计量数的比值越大,表示的反应速率越快,注意单位保持一致.
解答 解:不同物质表示的速率之比等于其化学计量数之比,故不同物质表示的速率与化学计量数的比值越大,表示的反应速率越快.
A.$\frac{v({B}_{2})}{3}$=0.267 mol/(L•s);
B.v(B2)=3mol/(L•min)=0.05mol/(L•s),$\frac{v({B}_{2})}{3}$=0.0167 mol/(L•s);
C.$\frac{v(C)}{2}$=0.3 mol/(L•s);
D.$\frac{v({A}_{2})}{1}$=0.4 mol/(L•s),
故反应速率D>C>A>B,
故选D.
点评 本题考查化学反应速率快慢比较,可以转化为同一物质表示的速率进行比较,比较基础.


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:解答题
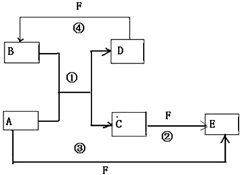 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出)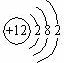 .反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O
.反应④的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 形成产物C和D的化学键放出的总能量高于断开反应物A和B的化学键所吸收的总能量 | |
| B. | 该反应只有在加热条件下才能进行 | |
| C. | 反应物的总能量高于产物的总能量 | |
| D. | 该反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
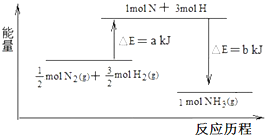 在化学反应中,反应物转化成生成物,必然发生能量的变化.
在化学反应中,反应物转化成生成物,必然发生能量的变化.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 面粉增白剂中的成份CaO2具有强氧化性 | |
| B. | CaO能与SO2反应,可用作工业废气的脱硫剂 | |
| C. | 新能源汽车的推广与使用有助于减少光化学烟雾的产生 | |
| D. | PM2.5是指空气中直径≥2.5μm的颗粒物,它们分散在空气中形成胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2+3H2$?_{催化剂}^{高温、高压}$2NH3△H<0,在任何温度下均为自发反应 | |
| B. | 向新制氯水中加入少量小苏打固体可提高其漂白能力 | |
| C. | 1L密闭容器中发生反应4NH3+5O2?4NO+6H2O,充少量 N2可加快反应速率 | |
| D. | 湿法炼铜的反应为Fe+CuSO4=FeSO4+Cu,反应中的Fe可以用Na代替 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 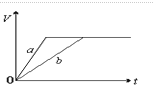 | B. | 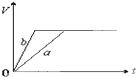 | ||
| C. | 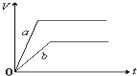 | D. | 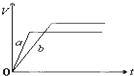 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com